질병 진단용 호흡가스 분석기술 동향
Trends in Breath Analysis Technologies for Disease Diagnosis
- 저자
- 김용준, 허재두 / 융합기술미래연구팀, 김승환 / 바이오의류IT융합연구부
- 권호
- 29권 5호 (통권 149)
- 논문구분
- IT 융합기술 특집
- 페이지
- 86-95
- 발행일자
- 2014.10.01
- DOI
- 10.22648/ETRI.2014.J.290509
- 초록
- 환자의 입 냄새로 질병을 구분했다는 기록은 고대 동서양의 역사에서 많이 찾아볼 수 있다. 최근 훈련된 개가 냄새로 암환자와 정상인을 구분했다는 뉴스가 보도 되었다. 호흡가스의 분석을 이용한 질병 검진은 병원에서 진행되고 있는 기존의 고가의 장비나 혈액 채취를 이용한 방법과 비교할 때 검진자와 피검진자가 손쉽게 저가로 진행될 수 있다는 장점이 있다. 최근 인체 호흡가스 분석법에 대한 연구개발이 미국과 유럽 국가를 중심으로 활발하게 진행되고 있다. 현재는 폐암, 폐결핵, 천식 등 주로 호흡기 관련 질병에 대한 분석법이 주를 이루고 있지만, 질병과 호흡가스 성분의 연관성이 밝혀짐에 따라 호흡가스 분석에 근거한 질병 진단은 미래의 다양한 질병 진단법으로 등장할 것으로 예상된다. 본고는 최근 호흡가스 분석법으로 응용되고 있는 질량 분석법과 가스 센서 어레이 기술의 현황 및 이들의 질병 진단 응용에 대해 전망하였다.
Share
I. 서론
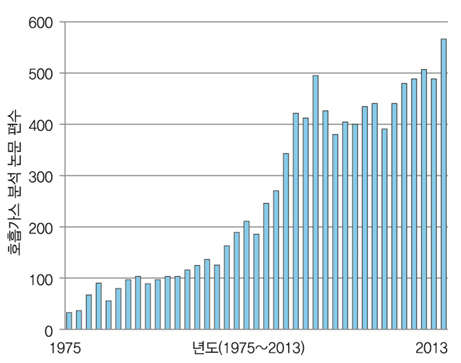
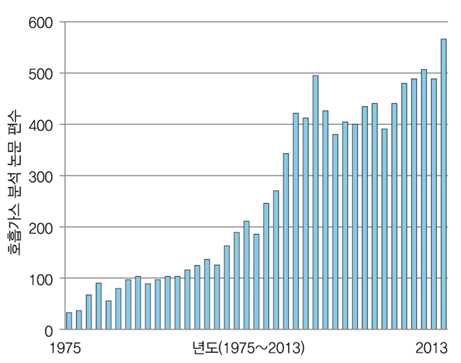
최근 인체 호흡가스 분석을 이용한 질병 진단에 대한 연구가 지속적으로 증가하고 있다((그림 1) 참조). 이는 기존의 병원에서 진행되는 검진방법이 일반적으로 고가의 장비를 필요로 하거나, 환자의 혈액이나 조직 채취를 필요로 하여 환자의 불편을 가중시키고, 검진결과까지 일정 시간이 걸리는 등의 단점이 있다. 그러나 호흡가스 분석에 근거한 질병 진단은 환자에게 편리하고, 저가 진단이 가능하며, 분석결과의 판단과정 또한 실시간으로 이루어질 수 있다는 장점이 있다.
고대 그리스시대의 의사들은 인체 호흡에서 발생하는 냄새로 질병을 구분했다는 기록이 있고, 최근에는 당뇨병 환자의 호흡가스에는 아세톤과 암환자에 있어서는 벤젠, 아이소프렌과 같은 다양한 탄화수소계 VOC(Volatile Organic Compound)가 정상인 보다 증가 또는 감소된다는 결과에 근거하여 이들 VOC와 질병과의 관련성이 발표되었다[1]. 이러한 호흡가스에 대한 분석은 1970년대 Pauling이 GC(Gas Chromatography) 분석을 통하여 인체 호흡가스에서 약 250종의 VOC가 포함되어 있음을 발표한 이후[2], 인체 호흡가스의 성분과 질병의 관계에 대한 많은 연구결과가 발표되고 있다. 인체의 호흡가스의 주성분은 산소, 이산화 탄소, 질소, 습기이고, 이밖에 수 ppm(ppmpart per million)에서 ppb(part per billion) 혹은 ppt(part per trillion) 수준의 다양한 VOC가 존재하며 이들 미량의 호흡가스는 인체의 신진대사 상태를 반영하기 때문에 질병에 걸린 사람과 건강한 사람을 구분하는 인자가 될 수 있다.
기존 질병 분석에서는 일반적으로 MRI(Magnetic Resonance Imaging), CT(Computed Tomography), PET(Positron Emission Tomography) 등 고가의 장비가 사용되고, 환자의 혈액을 채취하는 침습법이 사용되기 때문에, 환자에게 정신적·육체적인 불편함의 주요 원인으로 작용한다. 반면 호흡가스 분석은 손쉽게 저가로 실시간 진행이 가능한 장점에 기인하여 다양한 형태의 가스 분석방법이 응용 및 개발되고 있다. GC는 가장 전통적인 가스 분석기로 GC-MS(Gas Chromatography-Mass Spectroscopy)를 이용한 인체 호흡가스 분석이 주로 이루어져 왔고 최근에는 GC의 장점을 보완한 PTR(ProtonTransfer Reaction)-MS, SIFT(Selected Ion Flow Tube)-MS 등의 장비가 개발되어 임상에 응용되고 있다.
전통적인 가스 센서 분야에 있어서도 생체 후각을 모방한 다수의 센서로 이루어진 어레이 기술이 전자 후각, e-nose 등의 이름으로 질병 진단의 목적으로 연구개발되고 있다. 센서 어레이 기술은 기존의 단일 센서의 주요 단점인 선택성의 한계를 극복하고 다수의 화합물로 이루어진 감지 대상의 분석이 가능하다는 장점에 기인하여 유럽에서 식품업을 중심으로 많은 발전이 이루어져왔다. 이러한 센서 어레이 기술은 인체 호흡가스와 같은 다수의 VOC로 구성된 분석에 유리하기 때문에 최근 호흡가스 분석을 이용한 질병 진단 연구에 많이 응용되고 있다. 본고는 최근 본격적인 시작 단계에 접어든 인체 호흡가스를 이용한 질병 진단에 대한 전반적인 내용과 이들 질병 진단에 사용되는 인체 호흡가스 분석 기술의 동향을 기술하고 인체 호흡가스 질병 분석에 대한 미래를 전망하였다.
II. 질병 관련 호흡가스
인체 허파에는 약 3백만개의 폐포가 존재하며 이들은 매우 얇은 모세관 망으로 둘러 쌓여있어서 혈액 내의 이산화탄소(CO2) 공기 중의 산소(O2)가 손쉽게 확산을 통해 전달될 수 있는 구조를 갖고 있다. 이러한 독특한 구조로 인해 일반 성인은 허파는 평균 70m2의 표면적에 걸쳐서 혈액과 공기 사이에 상호 확산이 발생한다. 혈액은 인체에서 발생하는 생리현상과 신진대사 상태를 반영하는 화학물질을 포함하고 있고 이들 중 분자량이 적은 화합물은 호흡과정에서 폐를 통해 인체 호흡가스 성분에 포함되어 인체 밖으로 배출된다. 이러한 다양한 생체 반응을 거친 호흡가스에는 인체의 건강상태를 반영하는 다양한 VOC가 존재한다. 질병과 관계 있는 호흡가스로는 일산화질소(NO), 일산화탄소(CO), 과산화수소(H2O2), 아세톤 그리고 벤젠과 톨루엔을 비롯한 탄화수소 계열의 VOC 등이 있다. 이들은 천식, 만성폐쇄성질환, 폐암, 폐결핵 등 다양한 호흡기 질환을 비롯한 다수의 질병과의 연관성이 있음이 최근 호흡가스 분석 연구결과에 발표되었고 이들의 진단 응용성에 대한 연구결과가 다수 발표되고 있다.
1. 일산화질소(NO)
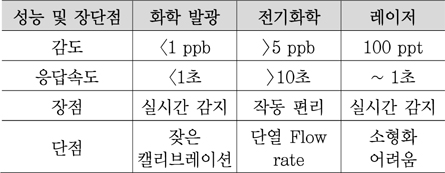
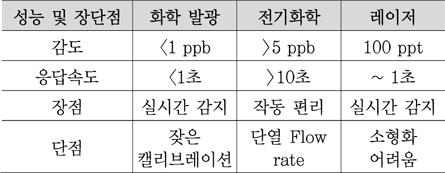
NO는 말초 혈류량, 혈소판 기능, 면역 반응, 신경전달, 염증매개체 등의 다양한 생체 기능과 연관성을 갖는다[3]. NO는 천식과 만성 폐쇄성 질환과 같은 기관지 염증 관련 환자에게 정상인보다 높은 농도로 발현되기 때문에, NO 농도 측정은 천식 및 만성폐쇄성 질환의 진단 및 이들 환자의 질병관리에 사용된다. 현재 NO 측정에 임상적으로 사용되는 표준 방법으로는 화학발광법이 있다. 이후에 개발된 측정법으로는 소형화에 유리한 전기화학에 근거한 방법과 레이저 기술을 이용한 방법이 있다. 이들 세 종류의 센서는 각각 장단점을 갖고 있다(<표 1> 참조).
화학발광 분석법에서의 NO 측정은 오존(O3)과의 화학반응에서 발생하는 광량을 측정하는 간접적인 방법으로 진행된다.
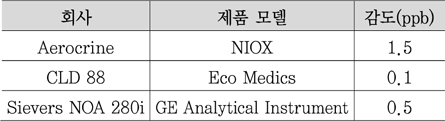
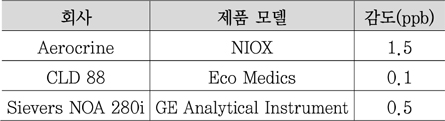
NO 측정용 상용화 제품은 몇몇 회사에서 출시되어 임상적으로 사용되고 있고, 이들 제품의 감지 한계는 일반적으로 ppb 수준에 이른다(<표 2> 참조).
대부분의 화학발광 분석기는 20~50kg 정도의 무게이며, 오존 생성에 필요한 공기 공급, 진공 펌프 등을 필요로 하기 때문에 비교적 고가이며 사용이 편리하지 못 하다. 또한 신뢰성 있는 결과를 확보하기 위해서는 주요 부품을 매년 점검해야 하고, 캘리브레이션을 매일 진행해야 하는 단점 등으로 인해 화학발광 분석법은 통상적 임상 분석이나 가정용 질병 모니터링 목적으로 적합하지 않다.
전기화학적 분석법에서는 가스의 농도가 전기적 신호로 전환되어 감지가 이루어지며, 일반적으로 저가와 소형화에 유리하다. 상용화 제품으로는 Aerocrine사의 NIOX MINO와 Bedfont사의 NObreath가 있고 이들은 FENO를 측정한다. 이들 센서는 hand-held 타입으로 1kg 미만이고 5ppb 수준의 감도로 화학발광법 사용화 제품과 비교할 때 10배 정도 떨어지지만 NIOX MINO 제품은 휴대용으로는 처음으로 2003년도에 FDA 승인을 받았다. 전기화학 센서는 비록 감도에 있어서 화학발광법에 뒤지지만 수 ppb 수준의 차이는 임상적으로 큰 문제가 되질 않는다. 소형의 전기화학 센서는 임상 분석에 적합하고 제작비용도 저렴하지만 일회 측정비용이 비싸다는 단점이 있다. NIOX-MINO의 경우 한번 측정에도 비용이 10달러 수준에 이른다.
광학적 방법에서는 빛이 분석 대상 분자와의 상호작용으로 인해 빛의 세기나 편광이 변하는 정도를 감지한다. NO 농도 측정용 광학 센서 기술은 오래되었지만, 인체 호흡가스 수준의 저농도 감지에는 TDLAS(Tunable Diode Laser Absorption Spectroscopy) 기술이 개발 된 이후 처음으로 이루어졌다[4]. TDLAS 기술에서는 레이저 빔이 multipass 셀을 통과하면서 여러 차례 반사되어 샘플과의 상호작용 거리가 늘어나 흡수 신호가 증폭되어 ppb 수준의 감도를 갖게 되었다. 그러나 레이저와 디텍터는 10~200K 수준으로 냉각을 필요로 하고 액체 질소 냉각기 내에서 작동해야 하기 때문에 실험실 외부에서의 작동에는 어려움이 있었다.
FRS(Faraday Rotational Spectroscopy) 기술에서는 빛이 자기장 내에 위치한 샘플을 통과하면서 발생하는 편광 변화를 측정한다[5]. 이 방법은 NO와 같은 상자성체만 감지 할 수 있어서 호흡 가스 중 NO만을 선택적으로 측정 가능한 장점을 갖는다. 1ppb 수준의 농도를 0.3초 수준에서 측정 가능하지만, 질소 냉각 시스템을 필요로 하기 때문에 측정 장소의 제약이 따른다.
1994년 QCL(Quantum Cascade Laser)이 소개되어[6] mid-IR 레이저의 소형화가 이루어지고 최근에는 모든 mid-IR 영역에서 상온 구동이 가능한 상용 소스가 등장하였고, 파장 모듈레이션 기술이 도입되면서 신호-노이즈율이 향상되어 0.2ppb 수준의 농도를 30초 수준에서 감지한다.
현재 임상용 NO 레이저 센서는 multipass방식으로 두 종류의 제품이 상용화되어 있다. EKIPS Technologies사는 액체 질소 대신 냉매를 이용한 ‘Breathmeter’를 출시하였다. 성능은 1.5ppb 수준의 농도를 4초에 감지 한다. 또 하나의 상용화 제품은 하나 이상의 분석 대상을 감지하기 위해 두 개의 QCL을 사용하여 0.3ppb 수준의 NO를 1초에 측정한다[7].
2. 일산화탄소(CO)
일산화탄소는 인체 내에서 헴(heme) 산화효소의 촉매 작용으로 발생된다[8]. 지난 수십년간 인체 내부 CO 가스 발생의 생리학적 의미에 대해 혈관 기능, 염증, 뉴런 시그널링에서의 역할과 이와 관련한 연구가 진행되어왔다. 최근에 와서는 CO가스는 천식, 만성폐쇄성 질환, 낭포성 섬유증, 기관지확장증 등의 질병과의 연관성이 알려지고, 중증환자와 수술 후 혹은 장기이식환자에 있어서 염증발생지표로 연구되었다. 또한 CO 측정은 흡연의 정도와 금연을 위한 방법으로도 사용되고 있다.
최근 저가의 범용 호흡가스의 CO 측정은 주로 사용과 소지에 편리한 전기화학 센서 방식으로 이루어지고 있으며, 시중에는 소형의 저가의 호흡 CO 센서가 다양하게 출시되고 있다. 최근 금연에 대한 사회적 인식이 고조됨에 따라 금연용으로 판매되는 경우가 많으며, 검출 범위는 대체로 ppm 영역(0ppm~200 ppm)이다. 실험실에서 주로 사용되는 호흡가스 CO 분석기는 ppb 수준의 검출 성능을 갖고 있다. 전통적으로 사용되어오고 있는 GC를 비롯해서 IR 레이저 분광기 등이 있다.
호흡 가스 CO 측정법에 있어서 표준화와 감도가 향상되고 있지만 질병 진단법으로서의 CO 수치는 아직 불분명하고 인체의 호흡기 관련 생리학적 신진대사적 규명이 더욱 뒤따라야 할 것으로 전망된다.
3. 과산화수소(H2O2)
과산화수소는 인체 내에서 Cytochrome P450 환원효소, NAPDH 산화효소, Xantine 산화효소 등에 의해 생성되고 Fenton 반응, Glutathione peroxidase 등에 의해 소모된다. 인체 내에서 이처럼 다양한 생체 반응의 경로를 거치며 생성과 소멸을 거듭하여 정상인의 경우 일정 수준의 과산화수소를 유지한다. 지난 수십년간 인체 호흡가스 성분 내의 과산화수소는 폐질환 표지자로서 연구가 되어왔다. 비록 생리기구학적으로 복잡하고 선택성이미흡다고 알려져 있지만, 호흡기 염증에 관련해서는 과산화수소가 일관성 있게 상승된 수치를 보인다고 알려져 있다. 또한 호흡기 환자의 치료 성공 여부도 호흡가스 내의 과산화수소 양과 밀접한 관계를 갖는다. 과산화수소는 발생의 원인이 다양하고 염증뿐 아니라 다양한 질병과도 연관성이 있기 때문에 진단 표지자로 적지 않은 논란이 있음에도 불구하고 천식과 만성폐쇄성 질환관련 표지자로 많은 연구가 진행되고 있다.
4. 그밖의 질병 관련 호흡가스
인체 질병관련 호흡가스에는 천식 및 만성폐쇄성질환과 같은 호흡기 염증관련 표지자로 인정되었거나 연구가 진행 중인 NO, CO, H2O2뿐만 아니라 폐암, 폐결핵, 신장질환, 만성질환과 연관성이 있는 것으로 알려진 다양한 VOC가 있다.
암모니아, DMA(dimethylamine), TMA(trimethylamine)과 같은 아민계열의 호흡가스는 말기 신장 질환과 관련이 있음이 SIFT(Selected Ion Flow Tube)를 이용한 분석으로 확인되었음이 보고되었으며[9], SIFT 분석을 이용한 TMA와 암모니아의 농도 변화에 근거하여 투석 시간을 최적화한 결과 또한 발표되었다. 아민계열의 호흡가스와 신장질환과의 연관성에 대한 신뢰도는 아직 임상적 응용 수준에는 이르지 못하고 있지만, 이들의 연관성에 대한 보다 면밀한 연구가 지속되고 있다.
아이소프렌은 신진대사로부터 발생하는 주요 호흡가스로 콜레스테롤 신진대사에 관련하기 때문에 호흡가스의 아이소프렌 농도는 지방장애에 대한 비침습 검출법으로 활용될 가능성이 높다. 그러나 호흡가스 후반부에 배출되는 아이소프렌 농도는 변화가 심하기 때문에 측정 시 주의가 요구된다.
호흡가스 내의 아세톤 농도는 당뇨, 심장 수술 이후 대사스트레스와 관련이 있고 체중 조절 프로그램에도 응용된 경우가 있다. 그러나 아세톤은 물에 용해도가 높고 호흡가스에서의 농도와 체내 농도와의 관계가 일정하게 나타나지 않는 경우가 있어서 이들에 대한 보다 면밀한 연구가 진행되고 있다[10].
III. 호흡가스 분석법
1. 질량 분석법(Mass Spectrometry)
가. GC-MS
수많은 서로 다른 VOC가 포함되어 있는 인체 호흡가스의 분석법으로 GC는 측정원리적 관점에서 많은 장점을 갖고 있기 때문에, 그 동안 인체 호흡가스 성분 분석의 대부분은 GC-MS로 진행되었다. GC는 측정 메커니즘상 분석 대상 물질이 분리 칼람을 지나면서 분자량에 따라 혹은 분석 대상의 극성 정도에 따라 분리가 진행된다. 분자량과 극성에 따른 분리 성능으로 인해 일반적으로 GC-MS는 호흡가스에 대해 가장 정확한 분석 정보를 제공하는 방법으로 인정되고 있다. 그러나 호흡가스를 정량화하는 과정에는 매우 세심한 주의를 요하며, 농도별 샘플을 준비하여 캘리브레이션을 진행해야만 신뢰도가 보장된다.
최근 GC-MS 관련 기술이 다양하게 발전되어 기능과신뢰도가 더욱 향상되었다. 감도, 소프트웨어, 농축 시스템 등에서 많은 발전이 이루어졌다. 특히 SPME(Solid Phase Microextraction)는 현장 검출이 필요할 때 매우 유용하게 사용되는 방법으로, SPME가 감지 대상에 노출되면 감지 대상 화합물이 추출 소재에 스며들고, 이를 직접 GC에 연결하여 분석을 진행시키거나 적당한 용매로 추출한 후 분석을 진행한다. SPME 의 주요 부분인 주사기 바늘 끝부분은 용융 실리카로 제작되고 금속 부분은 흡착물질로 코팅되어있다. SPME 파이버는 감지 대상을 흡수하기 때문에 SPME의 코팅재료의 선택이 분석결과에 직접적인 영향을 미치게 된다.미국의 Supelco사는 다양한 기능의 파이버를 판매하는데 특히 흡수 소재의 극성도에 따라 분류하여 판매하고 있다. 예를 들어 PDMS(Polydimethylsilane)는 비극성 소재로 비극성 샘플을 추출하기 위한 코팅 소재이고 PA(Polyacrylate)는 극성으로 분류되어 극성 샘플을 추출하는 목적에 사용될 수 있는 코팅 소재이다. PDMS/DVB(Divinylbenzene)는 양쪽성 소재로 구분된다. GC-MS는 특히 호흡가스 분석 분야에 많은 관심을 불러일으키고, 이 분야의 생성 이래 가장 많은 기여를 해온 분석기기이지만, 가스 분석 과정에서 호흡가스 포집용 봉지를 필요로 하고 특히 호흡가스와 같이 저농도 분석능을 필요로 하는 경우는 농축 시스템이 동반되어야 하는데, 이들 포집용 봉지나 농축시스템은 종종 실험적 에러를 발생시키는 원인이 되기도 한다. 이들 샘플 포집 과정과 농축 시스템 그리고 정량과정에 필요한 캘리브레이션은 GC-MS 기능의 다양성과 성능 향상에 기여를 하였지만, 동시에 전문적 경험과 세심한 주의가 동반되어야 한다는 것이 GC-MS의 주요 단점으로 알려져 있다. 최근 이들을 보완하는 MS에 근거한 새로운 분석 기술이 계속 연구개발되고 있다.
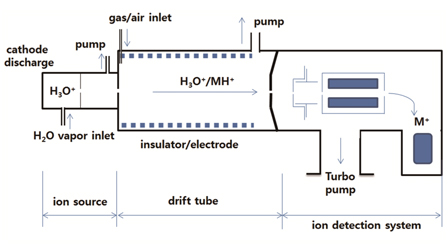
나. PTR-MS
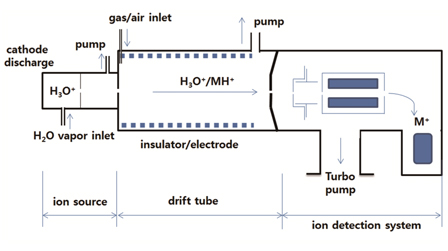
PTR-MS(Proton Transfer Reaction-Mass Spectroscopy)는 1990년대에 처음 개발되어 환경, 식품, 의학분야에서 VOC 모니터링용으로 사용되어 왔다[11]. 반응성 이온부터 발생한 양성자(H3O+)가 휘발성 분자(M)에 전달되는 반응으로 인해 이온화된 휘발성 분자(MH+)가 생성된다((그림 2) 참조).
이 이온화 반응은 ‘soft’ 이온화 방식으로 GC에서 사용되는 impact 이온화 방식과는 달리 MH+가 분해가 되지 않기 때문에 질량과 전하의 비율(m/z)로 간편하게 분석이 결정될 수 있으나 ‘soft’ 이온화 방식이 단점으로 작용하기도 한다. 두개의 서로 다른 화합물이 동일한 m/z값을 나타내는 경우는 구분이 어렵다. 이 경우 H3O+ 이온에 더불어 NO+와 O2+를 사용하여, 양성자화 반응의 동력학에서각 화합물을 특징적으로 발현하는 반응상수, kM값을 이용하면 분석이 가능하게 된다.
호흡가스 분석에 있어서 PRT-NS의 또 하나의 장점은 ppt 수준의 감도에 있다. 비록 대부분의 호흡가스 성분은 ppm 수준으로 존재하지만 호흡가스 중 질병과 관련하여 변화되는 정도는 ppb에서 ppt 수준에 이르기 때문에 ppt 수준의 초 저농도검출능은 질병 분석에 매우 유리하다.
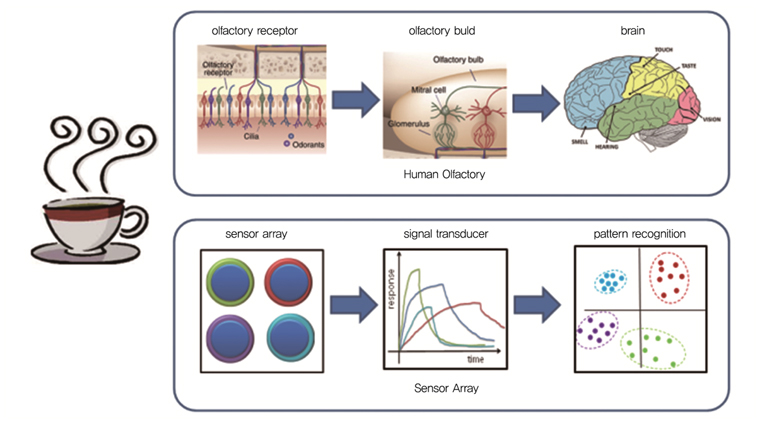
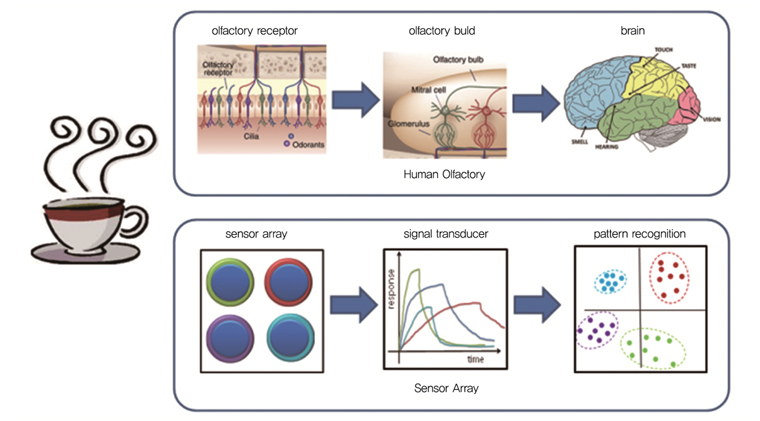
2. 센서 어레이 분석법
센서 어레이 기술은 다수의 화합물로 구성된 대상을 분석하려는 목적으로 1982년 Persaud의해 생체 후각 시스템을 모방하여 제작함으로써 시작되었다[12]. 인체의 후각시스템에는 수많은 감지리셉터가 존재한다. 개별적인 리셉터 하나 하나는 감지 대상에 대한 구분을 할 수 없지만 감지 성능이 서로 다른 다수의 리셉터는 감지 대상에 대하여 일종의 패턴형식으로 구분된다((그림 3) 참조). 같은 원리에 입각해서 센서 어레이 기술에서는 서로 다른 감지 특성을 갖는 다수의 센서를 어레이 형태로 사용하여 다수의 화합물로 구성된 감지 대상에 대해 패턴 형식으로 감지 대상 화합물이 구분된다. 센서 어레이 기술은 주로 유럽을 중심으로 와인 감별, 식료품 원산지 감별 등의 식품산업 분야에 주로 응용이 되며 발전해 왔다. 예를 들어 과일의 경우는 수많은 종류의 화합물로 이루어져 있으며 수확의 시기, 수확 당시의 일기 변화, 원산지 등 따라서 화합물의 구성이 달라지는 매우 복잡한 대상이기 때문에 기존의 분석기기인 GC와 같은 전문기기로 각각의 구성 화합물에 대해 하나 하나 분리하여 분석하기에는 현실적이 한계가 있다. 센서 어레이 기술을 도입하면 감지 대상 화합물의 성분에 대한 프로파일이 얻어지게 되어 마치 지문과 같은 인식이 가능하게 된다.
센서 어레이를 구성하는 기본 센서는 감지 메커니즘에 따라 혹은 센서 소재에 따라 다양하게 분류될 수 있는데 주로 상용되는 센서 소재로는 산화금속계, 전도성고분자, 카본 나노튜브, 금속 나노입자[13] 등이고, SAW(Surface Acoustic Wave) 센서와 QCM(Quartz Crystal Microbalance) 센서의 세서 물질로는 고분자 소재가 주로 사용된다. 센서 어레이의 성능은 구성 센서의 성능에 따라 주로 결정이 되고 패턴인식에 사용되는 알고리즘 또한 센서 성능에 주요한 영향을 미친다.
센서 어레이를 구성하는 단일 센서의 성능은 다양한 요소에 의해 결정되지만 특히 감도, 선택성, 안정성 이 센서의 세 가지 주요 성능으로 분류되고 있다. 이들 센서 본질적인 요소 이외의 중요한 센서 성능으로 실질적인 응용과 상용성 관점에서의 소형화, 저가, 사용 편리성이 또한 주요 성능 요소이다. 센서는 이들 성능요소들의 발전시키는 관점에서 다양한 감지 메커니즘과 다양한 감지 소재를 근간으로 발전해오고 있다.
이들 센서들의 주요 응용분야로는 자동차나 공장에서 발생하는 NOx, SOx, 탄화수소계 화합물, NH3, CO2 등의 환경 유해가스 감지, 화학전 및 테러에 사용되는 신경제와 같은 독성 화합물감지[14], 군사 및 테러용 폭발물 감지, 식품산업에서 숙성과정의 모니터링 등이 있다.
최근 인체 호흡가스와 질병과의 관계가 밝혀짐에 따라 의학분야에서의 질병 검진 등을 목적으로 매우 다양한 분야에서 사용되고 있다. QCM 센서 어레이를 이용하여 폐암 환자를 구분하였다. 검사 대상은 60명으로 이루어졌고 이중 35명의 암환자, 16명의 건강한 사람 그리고 9명의 수술을 받은 환자로 구성되었고, 이들 검사 대상들에 대한 구분이 100% 이루어졌다[15]. 이 밖에도 색변이 센서, 금나노 입자센서 어레이도 호흡가스를 이용한 암환자 구분에 사용이 되었다. 최근 센서 어레이 기술의 의료분야의 응용은 지속적으로 증가할 것으로 기대되며, 기존 센서 시장의 확대를 가속화시킬 것으로 예상된다.
IV. 국내외 기술동향
국내 KAIST의 김일두 교수팀에서는 산화금속 소재를 전기방사하여 나노섬유상의 센서를 제작하여 아세톤과 톨루엔 감지결과를 발표하였다[16]. 아세톤은 당뇨관련 호흡 표지자로 정상인의 호흡가스 중에 0.3~0.9 ppm 수준으로 존재하고 당뇨환자 경우는 1.8ppm 이상이 검출된다[17]. 톨루엔은 폐암환자에서 30ppb 수준으로 검출된다고 알려져 있다. 김일두교수팀이 발표한 검출 결과는 주어진 농도의 아세톤과 톨루엔 가스를 실험실에서 검출한 결과이다. 임상적으로 환자의 호흡가스를 검출하기 위해서는 센서 어레이 기술, 호흡가스 포집 등에 대한 연구가 부가되어야 한다.
중국의 Zhejiang 대학의 Chen은 SPME와 GC의 분리 칼럼 그리고 SAW 센서 어레이를 연결하여, 기존에 알려진 폐암 관련 11 종의 VOC에 근거하여 폐암환자를 구분하였다[18]. 패턴인식으로는 artificial neural network 알고리즘을 사용하였다. 11 종의 VOC로는 벤젠을 비롯한 4 종의 방향족 벤젠 유도체 화합물과, 3 종류의 포화 탄화수소계, 두 종의 불포화 탄화수소계, 그리고 2종의 알데하이드계를 선택하였다. 미국의 Cleveland Clinic Foundation 에서는 상용화 센서 어레이(Cyranose 320)를 이용하여 암환자 62명과 14명의 정상인으로 구성된 샘플군에 대해 71.4% 수준의 sensitivity와 91.9%의 specificity로 구분하였다[19]. 사용된 Ctranose 320 센서어레이는 32 종의 고분자-카본블랙 복합체 센서로 이루어져있다. 이와 같이 국외의 가스센서를 이용한 질병 진단기술은 임상 수준의 결과를 발표하고 있고 주로 폐암 진단을 대상으로 하였지만 최근 미국 및 유럽에서는 폐암뿐 아니라 유방암 등 호흡기 이외의 질병 진단 가능성에 대해서도 연구가 진행되고 있다.
V. 결론
호흡 가스분석을 이용한 임상 진단 및 치료 후 모니터링 기술은 비침습, 환자 편의, 저가, 실시간 분석 등의 장점에 기인하여, 최근 다양한 센서를 이용한 연구가 진행되지만 아직 시작 단계에 있다. 질량 분석법에 근거한 검출 기술을 중심으로 한 몇몇 기술은 높은 신뢰도를 바탕으로 임상 연구를 진행할 수 있는 수준에 있다. 그러나 이들 질량 관련 분석기기는 앞으로 소형화와 간단히 샘플링이 진행될 수 있는 방향으로 개발되어야 할 것으로 전망된다. 호흡가스 분석이 임상 검진으로 자리매김 하기 위해서는 호흡가스 성분과 질병과의 보다 면밀하고 광범위한 임상 연구가 뒷받침되어야 할 것으로 생각된다. 소형화와 사용의 편리성 면에서 유리한 센서 어레이 기술분야에 있어서는 산화 금속 센서, SAW 센서 및 다양한 나노 센서를 이용한 질병 진단 분석에 대한 연구가 진행되고 있다. 임상적으로 보다 신뢰성 있는 센서어레 기술 개발을 위해서는 고감도 및 고선택성 성능을 갖는 센서엘리먼트의 개발과 일관성 있는 호흡가스 샘플링법의 확보 등이 중요한 요소이다. 아직은 인체 호흡가스를 이용한 질병 진단이 초기 단계에 있지만, 지속적인 가스 분석기 개발과 센서 어레이 기술의 발전 그리고 인체 호흡가스와 질병과의 관련성에 대한 연구로 호흡가스를 이용한 간단하고 편리한 질병 검진 방법이 호흡기 관련 질병을 우선적으로 시작해서 다양한 형태에 질병 검진에도 응용될 것으로 전망된다.
용어해설
VOC(Volatile Organic Compound) 분자량이 적은 유기 화합물로 휘발성이 강한 특성을 지님.
FeNO 호흡가스 중 NO의 fractional concentration으로서 천식 등과 같은 기도 염증 측정법에 사용됨.
SAW 센서 고체결정 표면을 따라 진행하는 웨이브의 특성은 결정 표면에 물질이 흡착되면 표면파의 진폭, 속도, 등이 변하는데 이러한 특성을 이용하여 제작된 센서임.
전기방사 고분자 용액에 고전압이 부하되면 방사 팁과 나노 섬유 컬렉터 사이에 전기장이 발생하고, 발생한 전기장이 고분자 용액의 표면장력을 극복하면, 용액이 분사되어 나노섬유를 형성됨.
약어 정리
CT
Computed Tomography
DMA
dimethylamine
DVB
Divinylbenzene
FRS
Faraday Rotational Spectroscopy
GC-MS
Gas Chromatography-Mass Spectroscopy
MRI
Magnetic Resonance Imaging
PA
Polyacrylate
PDMS
Polydimethylsilane
PET
Positron Emission Tomography
ppb
part per billion
ppm
part per million
ppt
part per trillion
PTR
Proton Transfer Reaction
QCL
Quantum Cascade Laser
QCM
Quartz Crystal Microbalance
SAW
Surface Acoustic Wave
SIFT
Selected Ion Flow Tube
SPME
Solid Phase Microextraction
TDLAS
Tunable Diode Laser Absorption Spectroscopy
TMA
trimethylamine
VOC
Volatile Organic Compound
F. Rock, N. Barsan, and U. Weimar, “Electronic nose: current status and future trends,” Chem. Rev., vol. 108, 2008, pp. 705-725.
L. Pauling et al., “Quantitative analysis of urine vapor and breath by gas-liquid partition chromatography,” Proc. Nat. Acad. Sci. USA, vol. 68, Oct. 1971, pp. 2374-2376.
L.E. Gustafsson et al., “Endogenous nitric oxide is present in the exhaled air of rabbits, guinea pigs and humans,” Biochem. Biophys. Res. Commun., vol. 181, 1991, pp. 852-857.
K.L. Moskalenko, A.I. Nadezhdinskii, and I.A. Adamovskaya, “Human breath trace gas content study by tunable diode laser spectroscopy technique,” Infrared Phys. Technol., vol. 37, 1996, pp. 181-192.
A.R.W. Mckellar, “Mid-infrared laser magnetic-resonance spectroscopy Faraday Discuss,” Faraday Discuss. Chem. Soc., vol. 71, 1981, pp. 63-77.
J.B. McManus et al., “Pulsed quantum cascade laser instrument with compact design for rapid, high sensitivity measurement of trace gases in air,” Appl. Phys. B, vol. 92, 2008, pp. 387-392.
R. Tenhunen, H.S. Marver, and R. Schmid, “Microsomal heme oxygenase. Characterization of the enzyme,” J. Biol. Chem., vol. 244, 1969, pp. 6388-6394.
S. Davies, P. Spanel, and D. Smith, “Quantitative analysis of ammonia on the breath of patients in end-stagerenal failure,” Kidney Int., vol. 52, 1997, pp. 223-228.
C.S. Probert et al., “Volatile organic compounds as diagnostic biomarkers in gastrointestinal and liver disease,” J. Gastrointestin Liver Dis., vol. 28, 2009, pp. 337-343.
W. Lindinger, A. Hansel, and A. Jordan, “Proton transfer-reaction mass spectrometry (PTR-MS): on-line monitoring of volatile organic compounds at pptv levels,): on-line monitoring of volatile organic compounds at pptv levels,” Chem. Soc. Rev., vol. 27, 1998, pp 347-354.
K. Persaude and G. Dodd, “Analysis of discrimination mechanisms in the mammalian olfactory system using a model nose,” Nature, vol. 299, no 5881, Sept.1982, pp. 352-355.
Y.J. Kim et al., “Response Properties of the gold nanoparticle sensors toward benzene and toluene vopors,” IEEE Sensors 2006, EXCO, Daegu, Korea, pp. 1078-1080.
Y.J. Kim and J.D. Huh, “Nerve agents and their detection,” J. Sensor Sci. & Technol., vol. 22, 2013, pp. 249-255.
C.D. Natale et al., “Lung cancer identification by the analysis of breath by means of an arrayof non-selectivegas sensors,” Biosens Bioelectron, vol. 18, Sept. 2003, pp. 1209-1218.
J. Shin et al., “Thin-wall assembled SnO2 fibers functionalized by catalytic Pt nanoparticles and their superior exhaled-breath-sensing properties for the diagnosis of diabetes,” Adv. Funct. Mater., vol. 23, May 2013, pp. 2357-2367.
C. Deng et al., “Determination of acetione in human breath by gas cheromatography-mass spectrometry and solid-phase microextraction with on-fiber derivatization,” J. Chromatogr. B. vol. 810, Oct. 2004, pp.269-275.
X. Chen et al., “A study of an electronic nose for detection of lung cancer based on a virtual SAW gas sensors array and imaging recognition method,” Meas. Sci. Technol., vol. 16, 2005, pp. 1535-1546.
- Sign Up
- 전자통신동향분석 이메일 전자저널 구독을 원하시는 경우 정확한 이메일 주소를 입력하시기 바랍니다.