최은창 (Choi E.C) 의료IT융합연구실 실장
Ⅰ. 머리말
1987년 Charles W. Hull이 설립한 3D Systems사에서 세계 최초로 3D 프린터의 실용 기계를 발매한 이래 90년대 중반까지 세계적으로 다수의 기업이 3D 프린터 시장에 진입했다.
그런 흐름 속에서 2000년 전후에 ‘제1차 3D 프린터 붐’이 찾아온다. 당시에는 3D 프린터라 하지 않고, Rapid Prototyping(RP)을 위한 ‘RP장비’라고 불렀다. 그 당시에는 광조형 방식이 주를 이루었으나, 제1차 붐을 전후로 종이 적층조형 장치, 석고 분말을 착색하여 굳히는 방식의 3D 프린터, 로스트 왁스법을 활용한 잉크젯 방식의 적층조형 장치 등 여러 가지 기술 방식이 탄생했다.
제1차 붐 시절의 3D 프린터는 매우 고가였지만, 90년대 후반 Roland DG사의 ‘MODELA MDX-3’라는 소형 절삭 가공기가 100만원 내외의 가격으로 판매가 시작되면서 새로운 흐름을 일으키게 된다. 또한, 저가의 3D CAD 소프트웨어가 등장하여 데스크톱 패브리케이션의 서막을 알리게 된다. 그리고 2002년 MIT의 Neil Gershenfeld 교수의 주도로 시작된 FabLab을 통해 많은 사람이 개인 제조에 대한 기회를 제공받게 된다.
‘제2차 3D 프린터 붐’은 2007년경에 찾아온다. 이 시기에는 3D 스캐너로 스캔한 데이터를 3D 프린터로 출력하기까지의 일련의 흐름이 활발히 거론되었다.
2008년경 수지 용해 적층 방식으로 불리는 적층조형 기술의 특허가 만료됨에 따라, 오픈 소스 기반 3D 프린트가 시장에 진입하게 되고, 3D 프린터가 단번에 저가격화된 것이 하나의 원인이 되어 ‘제3차 붐’이 도래한다. 그리고 3D 프린터가 개인의 책상 위에 둘 수 있는 크기가 되고, 가격도 개인이 살 수 있게 됨으로써 제조의 세계도 크게 바뀔 것이라고 소개하고 있는 2012년에 출간된 Chris Anderson의 ‘Makers: The New Industrial Revolution’이 큰 주목을 이끌고, 2013년 미국 오바마 대통령이 국정연설에서 3D 프린터 보급을 위한 정책을 연달아 내놓음으로써 3D 프린터에 대한 관심이 급증하게 되었다.
우리나라는 2014년 4월 국가과학기술심의회에서 2020년 3D 프린팅 글로벌 선도국가로의 도약을 비전으로 하여, 3D 프린팅 기술을 제조업 혁신 및 창조경제 신시장을 창출할 핵심기술로 하여, 산업 생태계 조성을 위한 종합적인 육성 방안을 제시하기 위해 「3D 프린팅 산업 발전전략」을 수립[1]하고, 4대 추진전략과 11대 세부추진과제를 마련하여 정부주도 하에 적극적으로 육성하려 하고 있다.
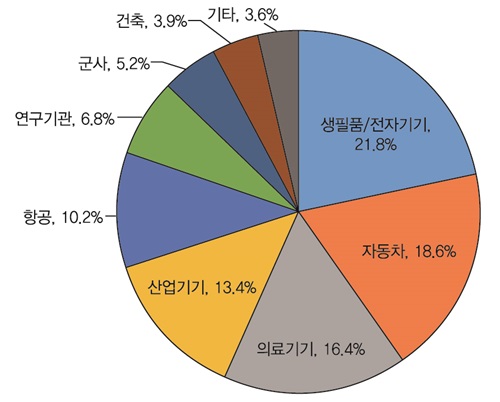
(그림 1)은 3D 프린터를 도입한 기업의 업종을 누계로 표시한 것이다. 생필품이나 전자기기 분야, 자동차 분야를 중심으로 모형이나 시작품 등을 제조하기 위해 3D 프린터를 활용하고 있으며, 의료의 경우는 보청기나 치과 보철물 등과 같이 주문 제작이 필요한 제품을 제조하기 위해 이용되고 있다. 3D 프린팅의 주 방법인 적층조형 방식을 활용하고 있는 의료분야는 전체 3D 프린터 사용분야의 16.4%를 차지하고 있다. 이는 의료장비가 필요로 하는 요건과 적층조형 기술이 제공하는 역량이 일치했기 때문이다. 예를 들어, 맞춤형 보청기, 치과 임플란트, 외과 임플란트와 같은 의료장비는 상대적으로 소형이어서 일반적인 적층조형 시스템을 통한 생산에 적합하다. 또한, 환자 개개인에 대한 맞춤화를 필요로 하는 점도 적층조형 기술과 잘 어울리는 특성이다. 또한, 적층조형 기술은 자연 세포조직에서 찾아볼 수 없는 조직 고정을 위한 생체 적합 물질이나 골격의 삽입 없이 세포 배양체를 구성할 수 있는 특성을 가지고 있다.
3D 프린팅 기술의 바이오분야에 활용된 것은 2000년을 전후로 수지 적층조형(FDM) 방식에 생체친화성/생분해성 고분자를 결합한 인공 지지체(synthetic scaffold)를 제작함에 따라 의공학 분야에 활용되기 시작했다.
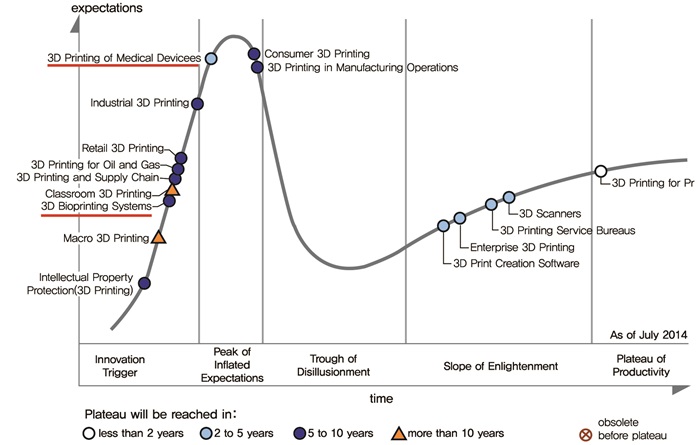
가트너의 하이프 사이클[(그림 2) 참조]에 따르면, 의료용 디바이스와 바이오프린팅 시스템에 활용되는 3D 프린팅 기술은 이제 막 도입이 되고 있고, 언론과 대중의 관심이 늘어나는 추세로 아직 기술의 잠재성으로 발생하는 기술 상품을 나타내는 발생기(technology trigger) 단계에 있다[3].
그리고 인간 세포를 연속적으로 층층이 쌓아 올려 살아 있는 세포조직을 구성할 수 있는 바이오 프린터에 대한 연구와 투자가 증가하고 있다.본고에서는 의료분야에서의 3D 프린팅 기술을 활용한 바이오프린팅에 대한 전반적인 연구개발 동향에 대해 알아본다.
Ⅱ. 3D 바이오프린팅 소재
본 장에서는 3D 바이오프린팅을 하기 위해 어떤 소재가 이용되고 있는지 알아본다.
1. 바이오프린팅에 사용되는 주요 소재
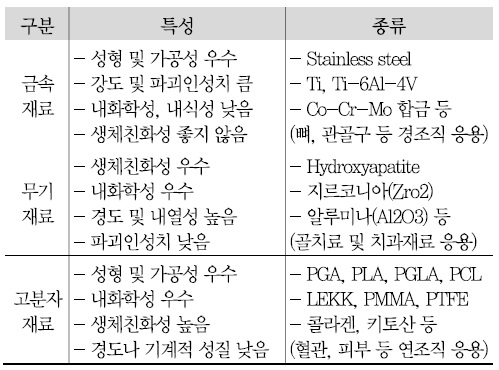
의료분야에서 사용되는 제품의 소재는 재질에 따라 <표 1>과 같이 금속재료, 무기재료, 고분자재료, 복합재료 등으로 구분할 수 있다. 개발하고자 하는 목적에 맞는 바이오 소재를 선택하고, 3D 프린팅 방식에 따라 프린팅하게 된다.
비생물학적으로 응용하기 위해 설계된 3D 프린팅 기술에는 일반적으로 살아있는 세포 및 생체 물질과 호환되지 않는 유기용제나 가교제 등이 사용된다. 따라서 프린팅 과정에서 생물학적 재료와 잘 호환될 뿐 아니라 원하는 기계적, 기능적 특성을 가진 조직구조를 제공할 수 있는 물질을 찾는 것이 3D 바이오프린팅 영역에서 주요한 쟁점 중 하나이다.
현재 자연적으로 유도된 중합체(동물 또는 인체조직에서 얻어진 alginate, gelatin, collagen, chitosan, fibrin and hyaluronic acid)나 합성 분자(polyethylene glycol)가 재생의학 분야에서 널리 사용되고 있다.
예를 들어, 인공혈관용 소재의 경우 혈관 내벽의 물성 및 화학적 특성, 물질전달 체계 등을 고려하여 열에 대해 안정적이고, 소독이 간편하며 뛰어난 소수성을 가진 Polytetrafluoroethylene(PTFE) 소재를 이용한다. 또한, 손상된 뼈나 경조직을 대체하고자 할 경우에는 스테인리스 스틸 또는 티타늄 소재를 이용하거나, 피부 재생에 이용하는 경우는 키토산(chitosan) 또는 콜라겐(collagen) 등의 바이오 소재를 이용하여 3D 프린팅 할 수 있다.
생체적합성이 뛰어난 키토산은 뼈세포의 활성을 자극하는 성질을 이용하여 뼈와 임플란트의 결합력을 높이는 코팅용으로 사용되고 있으며, 인산칼슘계 세라믹 물질인 수산화인회석(Hydrohyapatite)은 뼈 생장을 촉진하고 생체적합성과 골전도성이 좋아 골 대체물질로 활용되고 있다.
또한, 합성과정에서 친수성 및 흡수성의 합성 하이드로겔은 고유의 물리적 특성을 쉽게 제어할 수 있으므로 3D 바이오프린팅 재생의학 분야에 활용도가 높아지고 있다[4][5][6].
2. 생체조직 재생에 사용되는 소재
손상된 조직이나 장기를 교체하여 고유 기능을 회복시키려는 의학 분야를 재생의학이라고 한다.
2013년 일본 정부는 세계 최초로 induced Pluripotent Stem(iPS) 세포의 임상연구를 승인함에 따라 재생의학 분야에 대한 기대가 높아지고 있으며, 3D 프린팅 기술을 도입하여 재생의료에 활용하려는 움직임이 시작되고 있다.
현재 대표적인 사례가 iPS세포, ES세포, Mesenchymal Stem cells(MSC)를 이용한 것이다.
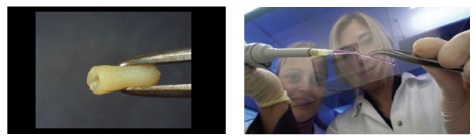
iPS(유도만능줄기세포)세포는 분화가 끝난 체세포에 세포 분화 관련 유전자를 주입하여 분화 이전의 세포단계로 되돌린 배아 줄기세포처럼 만능성을 유도해 낸 세포이다. 일본의 교토대학 iPS세포 연구소와 도쿄대학은 2003년 iPS세포와 3D 프린터를 사용하여 귀를 재생하는 프로젝트를 시작했다. CT 스캔에서 읽은 환자의 데이터를 바탕으로 귀의 연골 형태를 제작하고, iPS세포로 만든 연골 세포를 유입함으로써 귀를 재생한다. 또한, 오사카대학 등은 iPS세포로 만든 심근 세포와 혈관의 바탕이 되는 세포를 블록처럼 쌓아 혈관이 가진 심근 조직을 제작하고 있다[7].
Embryonic Stem(ES, 배아줄기세포) 세포는 인간 배아를 이용한 세포로, 미국의 코네티컷대학의 줄기세포연구소에서 ES세포를 사용하여 입체물을 인쇄하는 데 성공했다는 연구논문이 2013년 영국 물리학회(Institute of Physics)의 Biofabrication 학회지에 게재되었다. 아직 인간의 장기를 재현할 수 없는 단계이지만, 저항력이 약한 사람의 ES세포에 손상을 주지 않고 3D 프린팅이 가능한 방법을 입증하는 것이 이 연구의 목적으로, 실험실에서 배양한 인간의 ES세포가 포함된 액상의 바이오 잉크를 사용하여, 특별히 설계된 밸브식 프린터로 인쇄를 하였으며, 수백만의 세포를 몇 분 만에 인쇄할 수 있다고 한다[8].
MSC(중간엽 줄기세포)는 성체줄기세포인 다능성(multipotent) 세포로 뼈, 연골, 근육, 지방 및 섬유아세포로 분화할 수 있으며, 조직의 항상성(homeostasis)을 유지시켜주고 손상받은 조직을 치료할 수 있다.
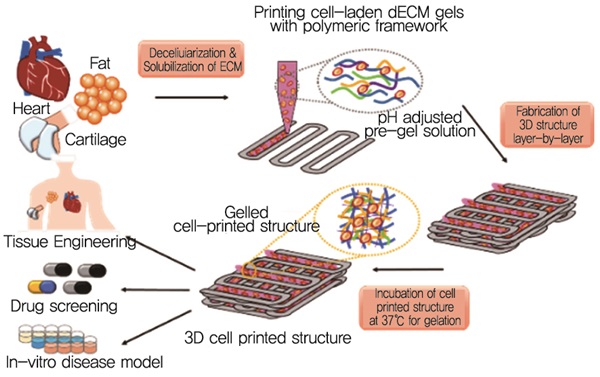
POSTECH 기계공학과 조동우 교수 연구팀은 실제 조직과 동일한 성분으로 이루어진 탈세포화된 조직으로 바이오 잉크를 만들고, 여기에 재생하고자 하는 조직에 맞는 중간엽 줄기세포를 넣어 3D 세포 프린팅 기술로 인공조직을 만들었다. 세포와 바이오 잉크를 섞어 고분자틀 사이사이에 분사하는 과정을 반복하여 3차원의 형상을 제작한다[(그림 3, 4) 참조][9][10].
Ⅲ. 3D 바이오프린팅 방법
1. 바이오프린팅 프로세스
3D 바이오프린팅 시스템은 인간의 장기와 같은 기능을 하는 조직과 모형을 생산한다. 그 프로세스를 보면, 한 개인 자신의 세포나 다른 세포로부터 제 기능을 하는 장기 또는 유용한 세포를 만들기 위한 프린팅 디바이스와 생체조직과 장기의 설계를 명시한 의료용 이미지 데이터 및 소프트웨어에 의해 관리된다.
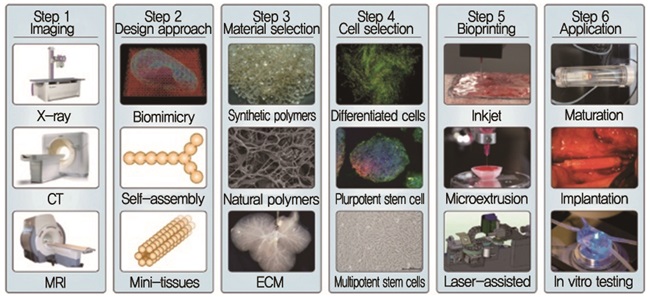
일반적으로 인공 보조물을 프린팅하기 위해서는 크게 3가지 단계를 거치는데, CT나 MRI와 같은 의료용 이미지를 가지고 3D 모델링을 한 후, 모델링된 데이터를 가지고 3D 프린팅이 가능한 파일(STL, Obj 파일 등)로 변환하여 신체 부위를 프린팅하고 후처리를 하게 된다[(그림 5) 참조]. 그 중, 세포가 포함된 바이오 잉크를 이용한 바이오프린팅 프로세스를 살펴보면 다음과 같다[(그림 6) 참조][12].
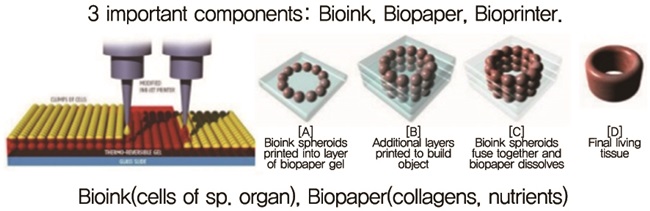
① 세포가 포함된 바이오 잉크를 형태 유지를 위한 바이오페이퍼(콜라겐, 젤라틴 등으로 구축) 배열
② 세포가 인쇄된 바이오페이퍼를 층층이 쌓아 올려 원하는 조직을 구성
③ 세포들이 융해될 수 있도록 프린트하는 동시에 자외선 등을 조사
④ 살아있는 조직 완성의 단계로 장기의 조직을 프린팅한다.
2. 간 조직 바이오프린팅
2013년 미국 샌디에이고에 있는 Organovo에서는 3D 프린터로 만든 간이 40일 동안 활동하도록 하는 데 성공했다[13].
Organovo에서 개발한 생체조직의 3D 프린팅 방법에 대해 알아본다.
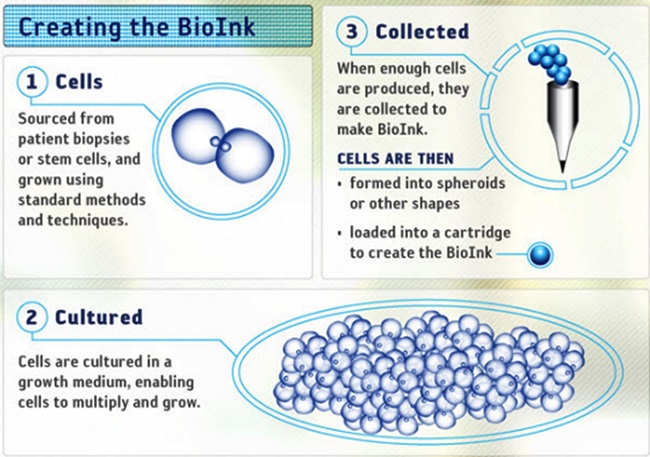
우선 생체조직을 인쇄하기 위한 방법을 설계한 뒤, 만들려고 하는 조직을 재생할 수 있는 다양한 세포들이 포함되어 있는 building block인 바이오 잉크를 이용하여, 앞서 설명한 바이오프린팅 프로세스와 같은 방식으로 3차원 조직을 만든다. 여기서는 하이드로겔을 지지체로 이용하고 있다[(그림 7) 참조].
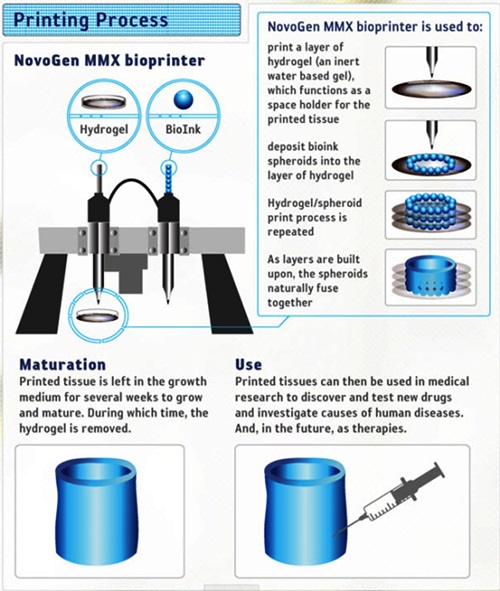
Organovo가 개발한 3D 바이오프린터 ‘노보젠 MMX’에 의한 간 조직 바이오프린팅 프로세스는 다음과 같다[(그림 8) 참조][13].
STEP1: 바이오 잉크를 주사기 하나에 채운다. 이 바이오 잉크는 수만 개의 간세포가 들어 있는 회전타원체들로 이뤄져 있다. 다른 하나의 주사기에도 바이오 잉크를 채우는데 여기에 주입되는 바이오 잉크는 세포성장을 촉진하는 비(非)간세포와 방출을 돕는 하이드로겔을 포함하고 있다.
STEP2: 바이오 프린터와 연결된 PC의 소프트웨어가 스테퍼 모터에 지시를 내리면 모터와 연결된 로봇 팔이 두 번째 주사기가 달린 펌프 헤드를 상하로 이동시키며 간 조직을 인쇄할 틀을 3D 프린팅한다. 이 틀은 육각형 3개가 벌집 형태로 나열된 모습을 하고 있다.
STEP3: 삼각측량 센서가 X축, Y축, Z축을 따라 움직이는 두 주사기의 바늘 끝 위치를 측정한다. 소프트웨어는 이 위치 데이터를 가지고 첫 번째 주사기의 위치를 결정한다.
STEP4: 로봇 팔이 첫 번째 주사기의 펌프 헤드 위치를 낮추면 주사기 속의 간 세포가 사출되며 벌집 모양의 틀을 채운다.
STEP5: 웰 플레이트(well plate)를 제거한다. 여기에는 최대 24개의 미세조직 완성품이 들어있는데 조직의 두께는 약 250µm다. 제거한 웰 플레이트를 배양기에 넣으면 세포들이 간 조직의 모습을 갖춰간다.
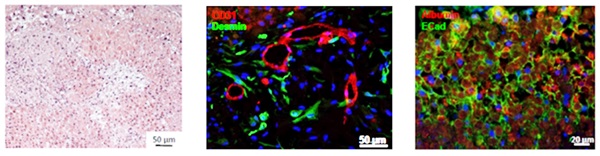
(그림 9)는 3D 바이오프린팅된 간 조직으로, 파란색으로 염색된 세포는 hepatocyte이고 빨간색으로 염색된 세포는 endothelial cell을 나타낸다. 그리고 녹색으로 염색된 세포는 hpatic stellate cell로 간 조직을 이루는 세포들이 한 곳에 모여 조직을 형성하고 있다[13].
Ⅳ. 3D 바이오프린팅 기술동향
CT나 MRI와 같은 의료영상으로부터 획득한 3차원 데이터를 이용하여 해당 장기나 조직 등을 3차원 프린팅하여 환자 맞춤형 서비스를 제공할 수 있다. 또한, 3차원 스캐닝으로 수술 부위를 재현하여 사전 수술 시뮬레이션을 가능하게 하여 수술 성공률을 향상시킬 수 있다. 현재는 맞춤형 보청기, 틀니, 치과 임플란트 등의 신체보조기기를 제작하거나, 인공 귀, 의족 보조기기, 인공 뼈, 인공 관절 등을 제작한 사례가 있다. 그리고 아직 초기 연구단계이나 향후 인공피부 조직이나 인공장기 등이 제작 가능할 것으로 예상된다.
유럽에서는 독일의 연구기관인 Fraunhofer Institute for Laser Technology의 주도로 3D 프린팅을 통해 인공혈관을 만드는 ArtiVasc 3D 프로젝트가 진행되고 있다[14]. 또한, Organovo사는 수만 개의 세포로 만들어진 바이오 잉크를 원하는 모양으로 적층하는 3D 프린팅 기술을 개발했으며, 인간 장기의 형태와 기능을 모방하는 살아 있는 인간 세포조직을 만들 수 있었다.
본 장에서는 유형별로 개발된 사례들을 소개한다.
1. 임플란트형
3D 프린팅 임플란트, 예를 들면 아래턱의 뼈는 지난 몇 년간 연구되고 있으나 실제 뼈로 대체하는 실험은 소수의 연구자만 수행하고 있다.
노팅엄 대학에서 연구하고 있는 Kevin Shakeshaff는 성체줄기세포를 코팅하는 폴리 유산과 젤라틴 상태의 알긴산 염류를 생성하는 바이오 프린터를 개발했다. Forbes에 따르면 뼈대를 분해하고 약 3개월 이내에 새로운 뼈의 성장으로 치환된다고 한다.
‘Osteofab’은 영국 ‘Oxford Performance Materials’라는 회사에서 의료용 임플란트(PEEK, PEK라는 열가소성 물질)에 이용되는 고성능 폴리머를 이용하여 만든 환자 맞춤형 두개골 지지체로, 2013년 2월에 미국인 남성 환자의 두개골 형상에 75% 맞게 모델링하고 3D 프린트해 만든 두개골 패치를 제조해 미국 식약청(FDA)의 승인을 얻었다[(그림 10) 참조][6].
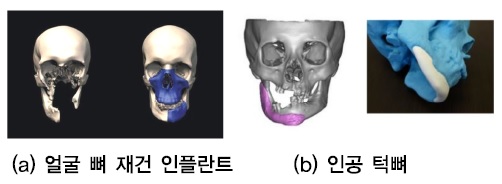
그 외 벨기에에서는 한 환자의 연조직과 얼굴 뼈를 이용하여 3D 프린팅된 임플란트를 사전 이식수술 가이드로 이용하였으며[(그림 11a) 참조], 3D 프린터로 만든 티타늄 보철물로 인공 턱뼈를 제작하여 턱관절 이식 수술에 성공한 사례가 있다[(그림 11b) 참조][15].
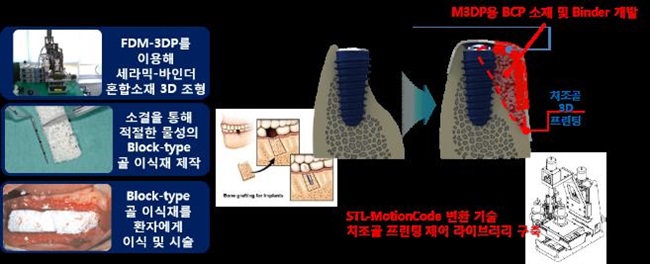
ETRI 대경권연구센터 의료IT융합연구실에서는 치조골 이식재를 3D 프린팅하는 기술 개발을 진행하고 있다[(그림 12) 참조]. 임플란트를 시술할 때, 치조골의 양이 부족할 경우 세라믹 소재의 인공골 입자를 이식해 넣어 신생골을 유도시킨 후 시술을 시작하게 된다. 이 경우 손실되는 입자의 양도 많으며 멤브레인 필터를 씌우는 고난도의 시술 과정 또한 동반된다. 하지만 3D 프린팅 기술을 이용해 치조골 이식재를 제작해 이식한다면, 재료비를 절감할 수 있으며, 멤브레인 필터가 필요하지 않기 때문에 시술 시간과 난이도가 감소하는 장점이 있다.
2. 체외 장착형
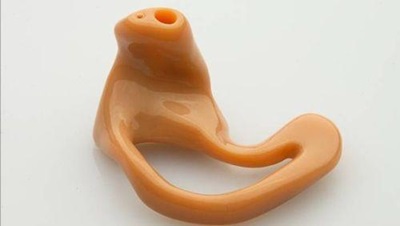
전통적인 맞춤형 보청기 제조과정은 주형제작에서부터 전자부품 조립과 최종 완성품이 나오기까지 총 10단계의 제조과정을 거치지만, 적층조형 방식을 이용함으로써 총 4단계(스캐닝, 모델링, 프린팅, 최종 조립)로의 축소가 가능하게 되었다[(그림 13) 참조]. 세계 최대의 보청기 제조업체이기도 한 독일 지멘스(Siemens)사 역시 적층조형 방식으로 전환 중에 있다[17].
의족이나 의수의 덮개를 맞춤형으로 제작하는데 3D 프린터를 활용하고 있으며, 환자의 체형에 맞게 제작할 수 있고, 금속이나 가죽 등 다양한 재질과 미관도 개인에 맞게 표현할 수 있다[(그림 14) 참조].
기존의 CNC 커팅으로 만들었던 Exoskeleton 타입의 의료용 보조기구 ‘WREX’를 ABS 플라스틱 소재로 3D 프린팅함으로써 보다 가볍고, 환자의 체형에 맞게 제조함으로써, 선천성근형성부전증(arthrogryposis multiplex congenital, AMC) 환자가 관절과 근육을 더욱 쉽게 움직일 수 있도록 하였다[(그림 15) 참조].
3D 프린터로 제작된 깁스로 초음파를 발생시켜, 그 진동을 이용하여 회복을 돕는 형태이다. 3D 프린터로 팔의 외형에 맞게 제작되며, 기존의 석고보다 진동을 전달하기 쉬운 소재로 되어 있다[(그림 16) 참조].
3. 장기 모델형
일본 고베대 외과 Maki Sugimoto 교수는 간암환자의 간을 형태적 특성과 생리적 특성(organ on a chip)에 따라 PVA 재질을 이용하여 실제 간과 같은 감촉의 3D 간을 제작하여 수술 전에 환자의 상태를 파악하는 데 활용하였다[(그림 17) 참조][21].
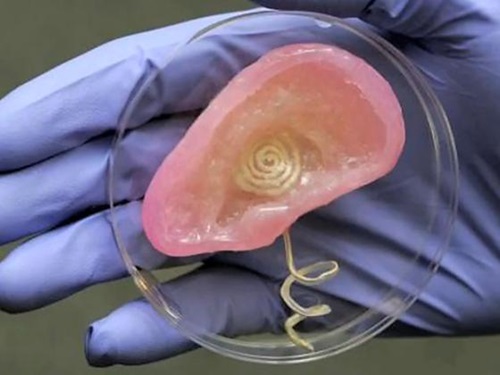
프린스턴 대학에서는 하이드로겔을 인간 세포와 함께 사람의 귀 모양으로 만들었으며, 달팽이관 모양의 전극부터 신호를 처리할 수 있게 은 나노입자 합금으로 만들어진 유도 코일을 내장시켰다[(그림 18) 참조][22].
코넬대 성형외과 Jason Spector 교수는 쥐 콜라겐으로 귀 모양을 성형하고, 송아지 연골세포를 주입해 배양한 다음, 쥐에 이식해 3개월간 배양하여 인공 귀를 제작하였다[23].
독일 프라운호퍼 연구소의 Günter Tovar 등은 합성 폴리머와 생체 분자의 혼합물을 사용하여 3D 프린트된 혈관을 만드는 ‘BioRap’이라는 프로젝트를 지휘하고 있다. 현재 동물 실험 중이며, 인체 실험은 아직 하지 않은 단계지만, 장기 이식도 3D 프린터로 실현할 예정이라 한다[(그림 19) 참조].
미국 MIT 및 펜실베니아대학에서는 옥수수에서 추출한 폴리머로 설탕 소재의 필라멘트를 코팅하고, 조직세포가 함유된 하이드로겔을 담체 안에 프린트한 후, 각 부분의 정착이 이루어지면 물로 씻어내어 설탕이 녹아 혈액세포가 지나다닐 수 있는 빈 통로가 생기게 하는 방식을 이용하여 혈관을 제조하였다.
새로운 피부를 프린팅하는 데 있어서 큰 문제는 사람마다 다른 피부 톤 밝기를 재현하는 것이 매우 곤란하다는 것이다. 왜냐하면, 사람의 피부는 매우 독특하고 얇으며, 변하기 쉽고 완벽한 복제본을 생성하는 것이 매우 어렵다.
웨이크 포레스트 대학에서는 화상 환자의 피부에 직접 프린트할 수 있는 기계를 미 국방성의 자금 지원을 받아 연구하고 있다.
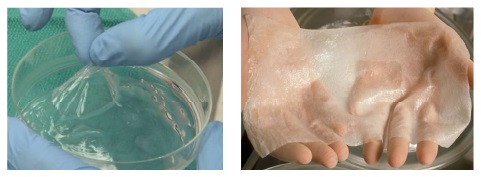
한편 리버풀 대학에서는 정밀하게 보정할 수 있는 3D 스캐너를 이용하여, 피실험자들의 피부 샘플을 채취하여보다 정확한 패치를 프린트하기 위한 연구를 진행하고 있다. 이 연구팀의 계획은 취득한 샘플을 가지고 ‘스킨 데이터베이스’를 만드는 것이다[(그림 20) 참조][25].
토론토 대학은 MaRS Innovations과 공동으로 모낭과 땀샘을 가진 이식 피부를 프린팅하는 3D 프린터를 개발하였다[26].
Ⅴ. 맺음말
현재 의료분야의 가장 큰 이슈는 환자 맞춤형 진료, 환자 맞춤형 시술/수술이라 할 수 있다.
바이오프린팅 기술의 발전으로 바이오 소재를 이용한 배양을 통해 인체 조직의 생산이 현실화된다면 의료 산업 혁신을 예상할 수 있다. 또한, 3D 프린팅 기술의 바이오 분야로의 응용은 차츰 그 영역을 넓혀 갈 것으로 기대하고 있다. 그러나 미국 식약청 등이 신체기관·장기의 바이오프린팅에 대한 사전승인제를 도입할 것으로 예상되면서 기술 진보와 기존 법 제도와의 갈등 이슈가 부각되고 있는 시점에서, 3D 프린트 제작물에 대한 임상 적용에 있어 인체 안정성 및 적합성의 문제와 법적 규제에 대한 기준안 마련이 우선되어야 하며, 3D 바이오프린팅 장치의 의료기기 인정 여부, 보험 적용 여부 등 정부차원의 선제적인 대응을 추진할 필요가 있다. 또한, 표준과 품질평가에 대한 방안 마련 등 해결해야 할 과제들이 많이 남아 있다.
References
(그림 1)
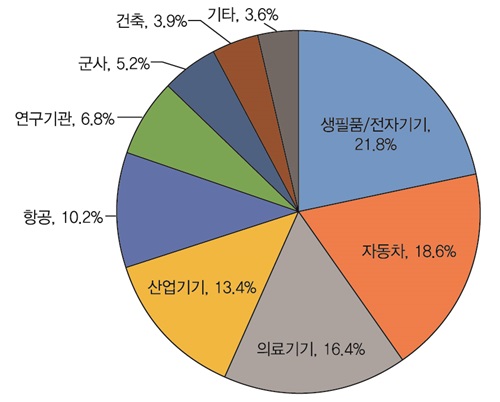
3D 프린터의 사용 분야<a href="#r002">[2]</a>
<표 1>
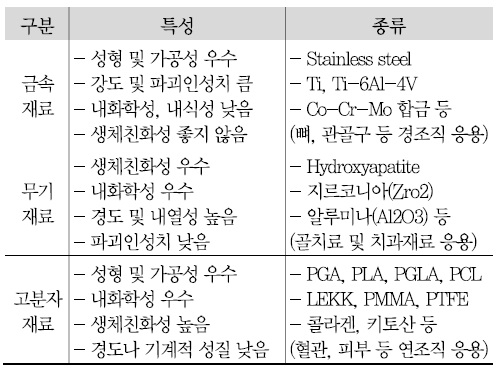
바이오 소재의 기능별 분류<a href="#r004">[4]</a><a href="#r005">[5]</a>
(그림 3)
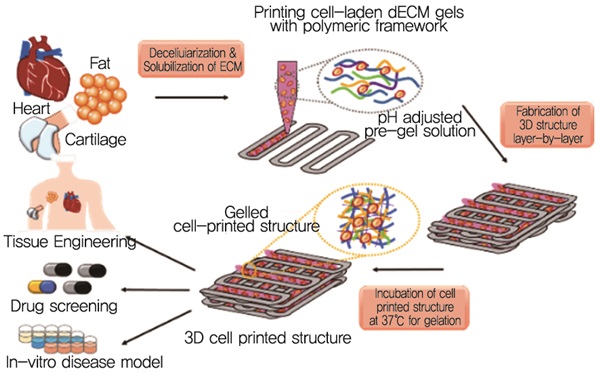
인공조직의 제작과정<a href="#r009">[9]</a>
(그림 4)

바이오잉크로 프린팅된 다양한 인공조직<a href="#r010">[10]</a>
(그림 5)
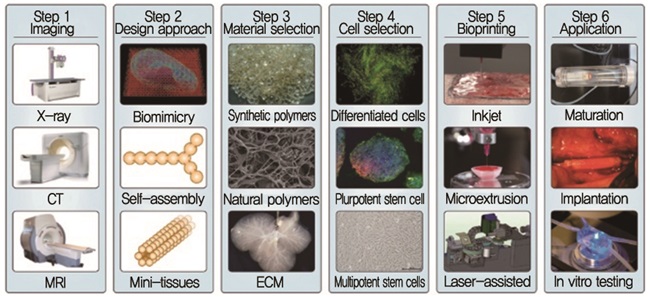
3D Bioprinting Process<a href="#r011">[11]</a>
(그림 6)
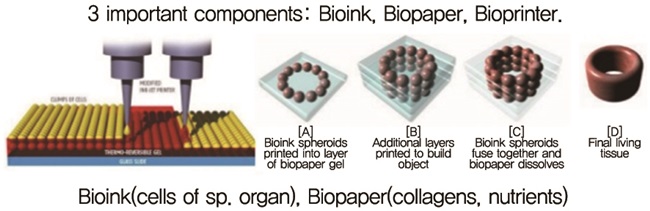
바이오잉크로 프린팅된 다양한 인공조직 프로세스
(그림 7)
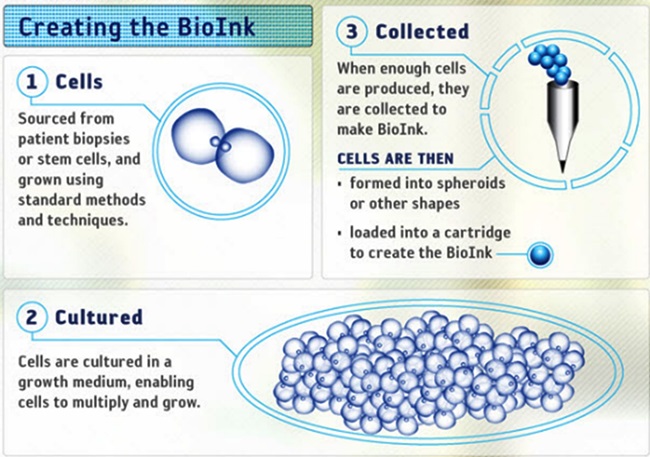
Creating the BioInk<a href="#r013">[13]</a>
(그림 8)
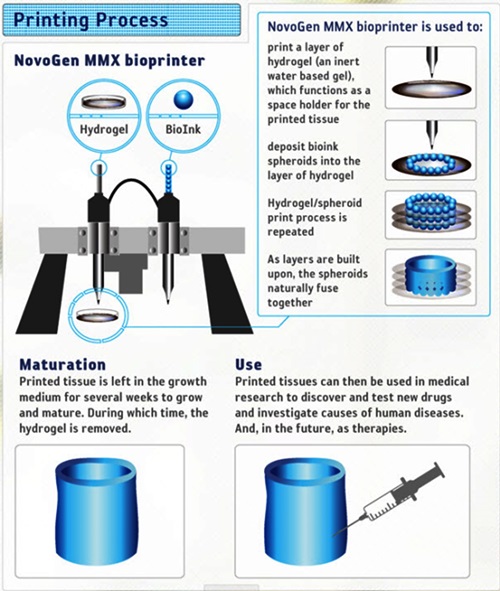
Printing Process<a href="#r013">[13]</a>
(그림 9)
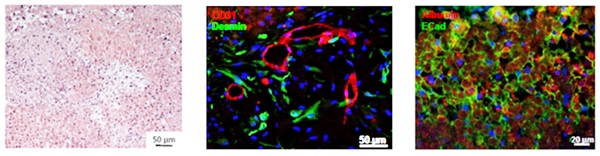
Histologic Structure in exVive3D Liver<a href="#r013">[13]</a>
(그림 10)

환자맞춤형 두개골 재건용 인공 지지체 ‘osteofab’<a href="#r006">[6]</a>
(그림 11)
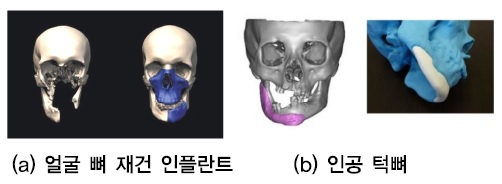
얼굴뼈 및 턱관절 임플란트<a href="#r015">[15]</a>
(그림 12)
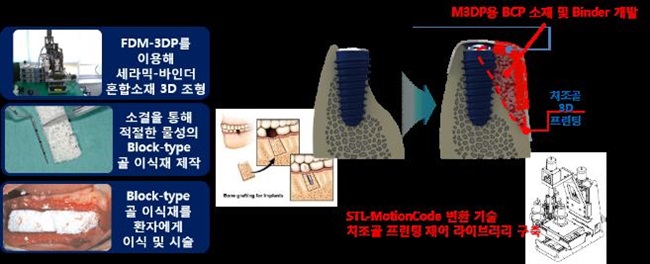
치조골 임플란트(ETRI)
(그림 13)
3D 프린터로 만든 보청기<a href="#r016">[16]</a>
(그림 14)

3D 프린팅 의족<a href="#r018">[18]</a>
(그림 15)

The ‘WREX’ Exoskeleton<a href="#r019">[19]</a>
(그림 16)

초음파 진동 깁스<a href="#r020">[20]</a>
(그림 17)

환자의 간 3D 모델<a href="#r021">[21]</a>
(그림 18)
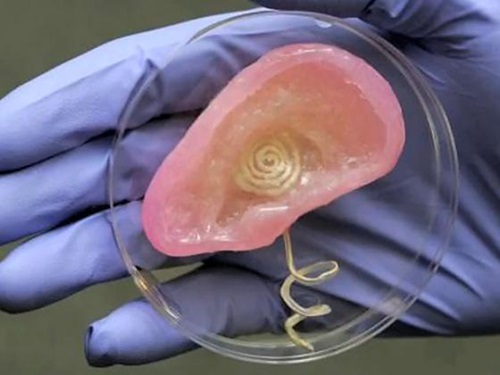
인공 귀(프린스턴대)<a href="#r022">[22]</a>
(그림 19)
인공혈관<a href="#r024">[24]</a>
(그림 20)
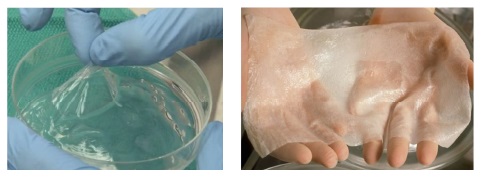
Skin Printing<a href="#r025">[25]</a>