이강찬 (Lee K.C.)
Ⅰ. 서론
인공지능(人工知能) 기술은 인간이 가진 지각, 학습, 추론, 자연언어 처리 등의 능력을 컴퓨터가 실행할 수 있도록 구현하는 기술로, 규칙기반 처리, 기계학습(머신러닝), 딥러닝, 자연어 처리, 음성인식, 시각인식 등과 같은 다양한 지능화 기술들을 통칭한다.
최근 딥러닝 기술을 중심으로 한 인공지능 기술의 비약적인 발전은 모든 분야에서의 인공지능 기술의 활용을 더욱더 촉진시키고 있다. 우리나라를 비롯하여 미국, 중국, 일본들에서는 국가적인 차원에서도 단순 신기술이 아닌 대변혁의 핵심 동력이자, 큰 잠재력을 가진 분야로 인식하고 기술경쟁력을 선점하기 위한 다양한 국가 정책을 추진하고 있다.
인공지능 기술의 이런 비약적인 발전의 배경에는 유무선 통신 기술, 클라우드, 빅데이터 기술 등과 같은 정보통신 기술의 발전, GPU, NPU 등의 하드웨어 기술의 발전, 그리고 머신러닝과 딥러닝 오픈소스와 오픈 데이터 등과 같은 개방형 기술 협력 체계들이 뒷받침하고 있다.
인공지능 기술은 핵심 기술의 빠른 진화를 하고 있는 것뿐만 아니라 제조, 금융, 교육, 농업, 항공 등과 같은 다양한 분야에서 생산성을 획기적으로 개선할 수 있는 범용 기술로 주목 받으며 다양한 산업 응용들에도 적용되고 있다. 특히 인류의 기본권 중 하나인 “건강”을 다루는 보건 의료 분야에서 인공지능 적용은 오래 전부터 시도되어 왔으나, 최근에는 인공지능 성능과 기술 진화에 필수 요소인 데이터의 축적 속도가 기하급수적으로 증가하면서 더욱더 빠르게 의료 인공지능 기술/시장의 성장 가능성과 활용 가능성이 높아져가고 있다[1].
의료 인공지능 기술은 특히 의료 분야의 현안으로 등장하고 있는 의료비 부담 증대, 의료 사고의 증대와 중환자실 안전 위험, 응급의료서비스에 대한 낮은 신뢰도, 낮은 의료 접근성, 의료 인력 부족 문제 등을 해결할 수 있는 대안으로 주목 받고 있다[3].
또한 의료 인공지능 기술은 축적된 의료 데이터들을 토대로 의료영상 판독, 질환 진단 예측 속도와 정확도를 높여 적시 치료를 가능하도록 하며, 나아가 신약 개발의 기간을 단축시키고, 의료 분야 난제들을 풀고 의료 비용을 절감하며 의료 서비스의 질적 수준을 높이는 혁신의 촉매제 역할을 할 것으로도 전망되고 있다[1-5].
본 고에서는 의료 인공지능에 대한 국제/국내 표준화 동향을 살피고, 새롭게 등장하고 있는 주요 이슈들이 핵심 인허가 체계와 어떻게 연계되는지를 검토하면서 국내 의료 인공지능 산업 활성화를 위해서는 앞으로 어떤 준비와 대응들이 필요할지를 살펴보고자 한다.
Ⅱ. 국제/국내 표준화 동향
1. 국제표준화 기구별 동향
가. ISO/IEC JTC1
ISO(International Organization for Standardization)와 IEC(International Electrotechnical Commission) 국제 표준화 기구의 합동 기술 위원회(Joint Technical Committee)인 JTC 1에서는 20여 년간 기본적인 IT 관련 표준화를 진행하여 왔다. 초기 단계에서 ISO/IEC JTC 1은 인공 지능 어휘, 인간 - 컴퓨터 상호작용, 생체 인식, 컴퓨터 이미지 처리 및 클라우드 컴퓨팅, 빅데이터 및 센서 네트워크와 같은 인공지능과도 연관된 주요 분야에서 표준 개발을 진행해왔다.
표 1 ISO/IEC JTC1 SC42 작업그룹 현황
인공지능과 관련하여 제정된 최초의 국제표준은 JTC1에서 1995년 12월 제정하였던 ISO/IEC 2382-28:1995 Information technology - Vocabulary - Part28: Artificial intelligence - Basic concepts and expert systems이다.
JTC1에서는 이후 1997년 12월에는 Part 31: Artificial intelligence - Machine learning, 1999년 8월에는 Part 29: Artificial intelligence - Speech recognition and synthesis, Part 34: Artificial intelligence - Neural networks 표준을 각각 제정하였다.
현재는 2015년에 개정된 ISO/IEC 2382:2015 Information technology – Vocabulary 표준으로 4종의 인공지능 용어 표준을 비롯해 총 31개의 다른 용어 표준들과 묶여 JTC1의 단일 용어 표준으로 통합 개정되었다.
JTC1에서는 이미 여러 그룹에서 인공지능 관련 기술들에 대한 표준화를 진행하고 있었지만, 상호 중복성 이슈 등을 해결하면서 인공지능 표준화를 총괄하는 새로운 표준 조직을 수립할 필요가 있다고 판단하게 되었다.
나. ISO/IEC JTC1 SC42
JTC1에서는 2017년 블라디보스토크 총회 의결을 통해 인공지능 관련 핵심 표준화를 위한 분과위원회(Subcommittee)를 신설하기로 결정하여 SC42가 신설되었다. 신규 분과 설립과 신규 표준안 2건을 제안했던 미국이 SC42의 간사국 지위와 의장직을 수임하였다.
2018년 4월 중국 북경에서 개최되었던 1차 총회에는 18개 P멤버(Participating Member)와 6개 O멤버(Observing Member) 중 17개국 86명이 참가하였고, SC42의 세부 구조 구성 및 업무 영역에 대한 협의를 진행하였다[6].
2018년에 4월에 열린 1차 회의를 통해 1개의 Foundational Standards WG(Working Group)과 3개의 SG(Study Group)을 구성하며 본격적인 활동을 시작하였다. 이후 2차(2018년 10월, 미국 산호세), 3차(2019년 4월, 아일랜드 더블린) 회의를 거치며 현재는 26개 P멤버, 13개 O멤버로 구성되며, 표 2와 같이 5개 WG과 1개의 JWG(Joint Working Group), 그리고 3개의 AHG(Adhoc Group)으로 운영되는 거대한 SC로 성장하였다.
현재 SC42의 각 WG별로 개발 중인 문서 및 담당 에디터들은 표 2와 같다.
표 2 SC42 제정 표준 및 표준 개발 현황
SC42의 활동 중 의료 분야 적용과 관련하여 관심 있게 볼 부분은 다음과 같다.
1) Risk Management (WG3)
WG3에서 작업 중인 ISO/IEC AWI 23894 Artificial Intelligence - Risk Management 문서는 인공지능 기술을 위한 위험관리 원칙과 프레임워크, 프로세스를 정리한다는 점에서 중요하다. 현재 작업 중인 문서에서는 Risk Management 원칙과 프레임워크, 프로세스를 정의한 ISO 31000 표준을 기반으로 인공지능 관련 추가 위험 요소와 확장 이슈들을 발굴하여 정의하는 방식으로 진행하고 있다.
의료기기 품질 관리를 위해 ISO 9001 표준과 연계한 ISO 13485(Medical devices - Quality management systems - Requirements for regulatory purposes)표준이 제정되었고, 의료기기 위험 관리를 위해 ISO 31000 표준의 응용 버전인 ISO 14971(Medical devices - Application of risk management to medical devices) 표준이 만들어진 것과 같이, 인공지능 기술을 위한 위험관리와 의료 인공지능 분야에서의 위험관리도 중요한 표준이 될 것으로 예상된다.
2) Ethical Issue (WG3)
WG3에서 TR(Technical Report) 형식으로 우선 작업을 시작한 윤리적인 이슈들을 다루는 두 가지 문서도 주목할만하다. 아직은 권고 사항들을 담을 수 있는 표준 문서로 성격이 적절하지 않기에 기술 문서로 작업을 하고 있으나, 이후 주요한 내용들이 추가적으로 논의되고 도출된다면 추가 표준을 만들 수도 있을 것으로 예상된다.
-
• ISO/IEC AWI TR 24368 - Artificial intelligence- Overview of ethical and societal concerns(인공지능의 윤리적 사회적 이슈들에 대한 개요)
-
• ISO/IEC NP TR 24027 - Artificial Intelligence(AI) - Bias in AI systems and AI aided decision making(인공지능 시스템과 인공지능 기반 의사결정 과정에서의 편향성)
특히 기계학습 기반의 모델인 경우, 학습 데이터의 종류와 양에 따라 의도치 않은 편향성이 발생될 수 있는 것처럼 자율적 지능화 처리의 수준이 높아지면서 인공지능의 윤리적 이슈는 더욱더 중요한 이슈로 부각되어가고 있다. 인공지능의 윤리적 이슈들은 자율성의 범위, 법적 책임 문제, 인간 권리침해 및 통제에 대한 이슈 등과 같은 다양한 영역들로 확산되고 있다[7,21].
EU의 GDPR(General Data Protection Regulation) 규제에 포함된 설명을 요구할 권리 규정과 자동화된 의사결정을 제한할 권리 등은 앞으로 인공지능 기술이 넘어야 할 또 하나의 큰 장벽이라고 할 수 있다. OECD를 비롯하여 국내에서도 차별 방지와 윤리 가이드라인 개발 등 신뢰 가능한 인공지능 구현에 대한 다양한 정책 개발을 추진 중에 있으므로 표준-제도를 연계하는 체계적이고 전략적인 대응이 필요하다[8-10].
3) Use case (WG4)
WG4에서는 다양한 인공지능 응용 사례들을 발굴하여 ISO/IEC NP TR 24030 - Artificial Intelligence (AI) - Use cases 문서로 정리하는 작업들을 하고 있다. 여기에는 제조, 서비스, 의료 등 다양한 분야들의 응용 사례들이 정리되고 있다.
다. ITU-T FG-AI4H
WHO(세계보건기구, World Health Organization)와 ITU(국제전기통신연합, International Telecommunication Union)는 건강 분야에서 인공지능 기술을 적용하는 과정에서 등장하고 있는 해석과 설명(interpretability and explainability) 불가능성의 해소, 신뢰성과 견고성(trustworthiness and robustness) 보장, 학습에 필요한 의료 데이터의 개인정보보호(privacy) 이슈, 그리고 성능 평가(performance evaluation)에 대한 방법과 절차 등과 같은 이슈들을 논의하고 관련 표준화 이슈들을 발굴하기 위해 2018년 7월 슬로베니아 Ljubljana에서 열린 ITU-T SG16 총회에서 2년을 활동 기간으로 하는 FG-AI4H(Focus Group on AI for Health) 그룹 신설을 결정하였다.
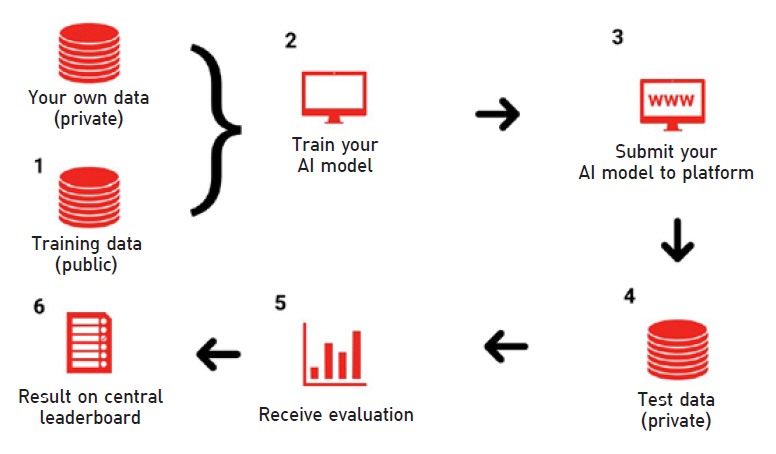
FG-AI4H는 건강을 위한 AI 기반 솔루션과 알고리즘들에 대해 그림 1과 같은 표준화된 평가방법을 만드는 데 주요한 초점을 두고 있으며, SNOMED CT(Clinical Terms) 또는 HPO(Human Phenotype Ontology) 코드, ICD(International Classification of Diseases)와 ICHI(International Classification of Health Interventions) 코드들과 같은 기준 치료 및 진단과 관련되는 기존 코드들을 표준 요소로 적극 활용하는 데도 깊은 관심을 갖고 있다[11].
FG-AI4H 그룹은 2018년 9월 25일부터 27일까지 스위스 제네바 WHO 건물에서 첫 번째 공개 워크숍과 회의를 개최하였다. 이후 다음과 같이 현재까지 총 5번의 공개 세미나와 대면회의를 개최하여 왔고, 2020년 1월까지 3회의 회의와 워크숍을 더 개최하기로 예정되어 있다.
-
• 1차 2018년 9월 25일(워크숍), 26~27일(회의) - 스위스 제네바, WHO
-
• 2차 2018년 11월 14일(워크숍), 15~16일(회의) - 미국 뉴욕, 컬럼비아 대학
-
• 3차 2019년 1월 22일(워크숍), 23~25일(회의) – 스위스, Lausanne, EPFL SwissTech Convention Center
-
• 4차 2019년 4월 2일(워크숍), 3~5일(회의) – 중국 상하이
-
• 5차 2019년 5월 29일(워크숍, AI for Good 공동), 30~31일, 6월 1일(회의) – 스위스 제네바
-
• 6차(예정) 2019년 9월 2일(워크숍), 3~5일(회의) – 탄자니아 Zanzibar
-
• 7차(예정) 2019년 11월 – 인도 뉴델리
-
• 8차(예정) 2020년 1월 – 브라질 브라질리아
FG-AI4H는 총 5개의 WG을 구성하여 이슈들을 논의하고 있다.
4월 상하이에서 열렸던 미팅에서 총 6개의 adhoc group을 운영하기로 결정하였다.
-
• AHG on test data set assessment - Co-chairs: Arun Schroff (MedIndia, India), Wojciech Samek (Fraunhofer HHI)
-
• AHG on thematic classification scheme - Chair: Ramesh Krishnamurthy (WHO)
-
• AHG Benchmarking Platform (AHG-BP) - ToR in D-035, Chair: Markus Wenzel (Fraunhofer HHI, DE)
-
• AHG AI for health device security and robustness benchmarking (AHG-AI4HDS) - Co-chairs: Ziyi Yang (CAICT, China) & Kai Fu (China Telecommunications Technology Labs, China)
-
• AHG working group methods for online collaborations - Chair: Benjamin Muthambi (Watif Health, South Africa)
-
• AHG Data handling and data acceptance policy (AHG-DAH) - Co-Chairs: Benjamin Muthambi (Watif Health, South Africa) & Daidi Zhong (Chongqing University, CN) & Marc Lecoultre (Wazzabi, CH)
표 3 FG-AI4H 작업그룹 현황
3차 회의부터는 AI 응용별 유즈케이스를 명확하게 하고 데이터 수집과 벤치마킹 방법 등을 정리하기 위해 표 4와 같이 14개 TG(Topic Group)들로 나누어 활동하고 있다.
표 4 Topic Group 현황(2019년 7월 3일 기준)
ITU-T의 FG(Focus Group)은 표준 문서를 직접 개발하지는 못한다는 한계를 갖고 있지만, WHO의 기본 철학처럼 선진국과 후진국을 모두 아우르는 의료 인공지능 분야별 유즈케이스를 개발하며 평가 체계를 만들려는 노력은 상당히 의미 있는 활동이라 할 수 있다.
1차 회의기간 전체 참석자가 103명, 2차 회의 참석자가 96명, 3차 회의 142명, 4차 회의 61명에 이르는 것처럼 의료 전문가들의 참여와 교류도 활발하게 이루어지고 있다. 앞으로 남은 기간 동안 주요 응용별 TG들을 통해 관련 전문가들을 모으고, 계획하였던 개방형 데이터의 발굴, 시험 방법 정리, 벤치마킹 플랫폼의 시범 운영 등을 진행할 예정이므로 앞으로도 관심 있게 지켜보면 적극적인 관심을 가질 필요가 있다.
라. ISO/IEC JTC1 WG12
3D 프린팅과 스캐닝 관련 표준화를 위해 JTC1 산하에 2017년 10월 신설된 WG12에서도 인공지능 관련 표준 개발을 추진 중에 있다. WG12에서는 ICT 기술이 결합된 3D 프린팅과 스캐닝 핵심 표준 개발을 비롯하여 의료/국방/DIY 등의 다양한 응용 분야 3D 프린팅과 스캐닝 관련 응용 표준 개발을 목표로 하고 있다.
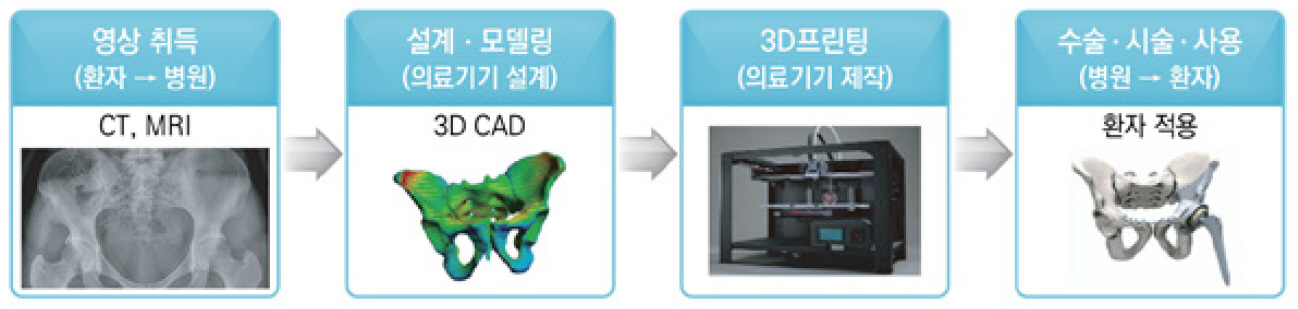
그림 2[12]와 같이 의료 3D 프린팅을 위해서는 환자 의료 영상을 기반으로 한 2D/3D 변환 과정을 거쳐야 하고, 이를 통해 3D 모델을 만들게 된다. 이 과정에서 다양한 3D 프린팅 소프트웨어 환경에서 의료 영상에 대한 분할 및 최적화를 위해 다양한 기술과 방법들이 적용되고 있어, 이에 대한 딥러닝 기반의 표준화된 분할 절차와 방법에 대한 표준 개발을 추진하고 있다.
표 5 WG12에서 추진(또는 계획) 중인 표준
WG12에서 표준화 진행 중이거나 향후 추진 계획을 갖고 있는 표준들은 표 6과 같다.
치과용 의료기기, 인체이식 의료기기, 수술용 가이드, 맞춤형 치료물 등을 모델링하고 제작해야 하는 의료 3D 프린팅 분야에서는 의료 영상 기반의 처리가 필요하기에, 이 과정에서 딥러닝 기술을 기반으로 하는 다양한 표준화가 추가 진행될 것을 보인다.
이 밖에도 3D 프린팅 모델에 대한 구조 역학적 분석, 포인트 클라우드 기반의 3D 스캐닝 포맷, 3D mesh optimization 등과 같은 다양한 3D 모델 최적화를 위한 딥러닝 기반의 기술 표준 개발도 예상된다.
Ⅲ. 인허가 관련 기준 규격 및 가이드라인 현황
1. 식품의약품안전처
아직 인공지능 기반 의료기기에 대한 국제적인 표준과 기준 규격은 없는 상태이기에 국내 식품의약품안전처에서는 국내 고유의 기준 규격과 허가 심사 체계를 만들어 운영하고 있다.
인공지능 기반 의료기기가 빠르게 발전하고 확산됨에 따라 앞으로 각 국가별 인허가 체계와 기준 규격들에 대한 국제 조화에 대한 필요성과 국제 표준 제정에 대한 필요성도 함께 늘어날 것으로 예상된다[13-15,17].
가. 인공지능 기반 의료기기에 대한 정의
식품의약품안전처에서는 인공지능 기반 의료기기를 다음과 같이 인공지능 기술을 사용하는 소프트웨어 의료기기(SaMD: Software As Medical Device) 형태로 규정하고 있다[13].
-
• 인공지능(AI) - 컴퓨터 기술을 이용하여 인간의 지능(지각, 추론, 학습, 이해 능력 등)을 수행할 수 있도록 구현하는 기술
-
• 의료용 빅데이터 - 진료기록 또는 의료기기로부터 측정된 생체 측정정보, 의료영상, 유전 정보 등 질병을 진단 또는 예측하기 위해 사용되는 다양한 의료정보
-
• 인공지능 기반 의료기기(소프트웨어) - 인공지능으로 의료 데이터를 분석하여 질병의 진단 또는 예측 등을 목적으로 하는 독립형 소프트웨어 형태의 의료기기
더불어 기계학습 방식의 인공지능 기반 의료기기는 기존 의료기기와 달리 4가지 차이를 갖는 것으로 명시하고 있다[13].
-
• 기계학습 방식은 소프트웨어가 의료용 빅데이터를 학습하여 질병의 특징을 스스로 도출하는 방식(그림 3)
-
• 의료진이 빅데이터 및 인공지능 기술이 적용된 의료기기에 환자의료정보를 입력하면 소프트웨어에 의해 도출된 질병의 특징을 이용하여 보조진단 결과를 출력
-
• 기존의 의료영상 분석·검출 또는 진단보조에 사용하는 의료용 소프트웨어와는 달리, 사용자 또는 제조자가 학습 데이터를 반영할 수 있어 진단 알고리즘이 실시간으로 변경 가능
-
• 클라우드 컴퓨팅 기술을 적용하여 네트워크를 통해 의료기관 자체 또는 외부의 클라우드 서버에서 데이터를 저장하거나 사용할 수 있음
나. 허가심사 기준 및 가이드라인

식품의약품안전처에서는 이러한 인공지능 기반 의료기기에 대한 허가/심사를 촉진시키기 위해 2종의 허가 심사 가이드라인을 발간하였다.
-
• 빅데이터 및 인공지능(AI) 기술이 적용된 의료기기의 허가·심사 가이드라인(민원인 안내서, 2017.11)
-
• 인공지능(AI) 기반 의료기기의 임상 유효성 평가 가이드라인(민원인 안내서, 2017.12)
다. 등급 분류 및 품목 분류
인공지능 기반 의료기기에 대한 등급 분류는 「의료기기법」 제3조(등급분류와 지정)에 따라 의료기기의 사용목적과 사용 시 인체에 미치는 잠재적 위해성의 차이로 분류된다. 품목분류는 사용목적, 특성, 위해도 등을 종합적으로 고려하여 「의료기기 품목 및 품목별 등급에 관한 규정」에 따라 분류된다.
현재 인공지능 기반 의료기기는 의료영상을 이용하는 형태와 의료정보를 분석하는 형태로 구분 가능하지만, 의료영상 기반 인공지능 의료기기들에만 품목 분류가 표 6과 같이 명시되어 있다[13].
표 6 의료영상을 이용한 빅데이터 및 인공지능 기술이 적용된 의료기기의 품목 예시
의료영상 이외의 의료정보를 이용하는 형태는 현재 「의료기기 품목 및 품목별 등급에 관한 규정」에 적절한 품목 분류가 없어, 표 7과 같이 추후 분류하여 관리할 예정으로 있다[13].
표 7 의료영상 이외의 의료정보를 이용한 빅데이터 및 인공지능 기술이 적용된 의료기기의 품목(안)
라. 성능 및 임상적 유효성 검증 항목
빅데이터 및 인공지능 기술이 적용된 의료기기의 성능 및 임상적 유효성 검증은 민감도(Sensitivity), 특이도(Specificity), 양성 예측도(Positive Predictive Value), 음성 예측도(Negative Predictive Value), ROC(Receiver Operating Characteristic) Curve, AUC(Area Under the Curve) 등의 항목을 이용하여 제품의 진단에 대한 정확도를 확인할 수 있다[13].
-
• 민감도(Sensitivity): 실제로 특정한 질병에 걸린 사람들 중에서 그 질병이 있다고 분류해내는 확률
-
• 특이도(Specificity): 실제로 특정한 질병이 없는 사람들 중에서 그 질병이 없다고 분류해내는 확률
-
• 양성 예측도(Positive Predictive Value): 특정한 특성을 갖고 있는 것으로 분류된 사람들 가운데 실제로 그 특성을 갖고 있는 사람이 차지하는 분률
-
• 음성 예측도(Negative Predictive Value): 특정한 특성을 갖고 있지 않는 것으로 분류된 사람들 가운데 실제로 그 특성을 갖고 있지 않는 사람이 차지하는 분률
-
• ROC(Receiver Operating Characteristic) Curve: 진단검사 결과를 근거로 민감도와 위양성률(1-특이도)을 이용하여 그린 그래프로, 양성과 음성을 구분하는 진단의 성능을 평가할 수 있음
-
• AUC(Area Under the Curve): ROC Curve의 아래 면적으로 진단 정확도를 의미하고 0.5~1.0 사이의 값에서 1에 근접할수록 이상적인 성능이라고 할 수 있음
성능 및 임상적 유효성 검증에 사용되는 데이터는 객관성을 유지하기 위하여 개발 데이터와의 상호 독립성 등을 고려하여야 한다. 더불어 체계적인 임상검증 노력들도 필요하다[20].
마. 버전 관리
빅데이터 및 인공지능 기술이 적용된 의료기기의 버전 관리 규칙은 제조자에 의해 제품의 구조, 설계 등을 관리하는 부분과 학습 데이터의 추가 등을 관리하는 부분으로 구분할 수 있으며, 변경 사항별 관리 방법은 표 8과 같다[13].
2. IMDRF SaMD 연관성
국내의 경우 SaMD에 대한 특별한 관리 기준 규격을 정의하고는 있지 않지만, 주요 국가별 규제 당국자들의 포럼인 IMDRF(International Medical Device Regulators Forum)에서 정의한 4건의 IMDRF주요 기준 규격 체계와 유사한 철학으로 운영하고 있다.
SaMD 위험도에 대한 분류 체계는 다음의 표 9와 같이 제공 정보의 유형과 위험도에 기반하여 1~4등급의 분류를 할 수 있다[14, (IMDRF/SaMD WG/N12 표준)]
Ⅳ. 핵심 정책 및 표준화 이슈, 시사점
지금까지 살펴본 다양한 정책 및 표준화 동향들을 통해 다음과 같이 8가지 주요 법/제도 및 표준화 이슈들이 있음을 확인할 수 있었다[1,3-5,7,15,16].
(1) 인공지능 기반 의료기기의 정의와 분류 체계
(2) 위험 관리 – ISO 14971
(3) 성능 평가(Performance Assessment)
(4) 표준 데이터 및 인허가 기준 데이터
(5) 임상 평가(Clinical Evaluation)
(6) SW 품질 관리 – ISO 13485
(7) 보안 및 프라이버시
(8) 윤리적 이슈
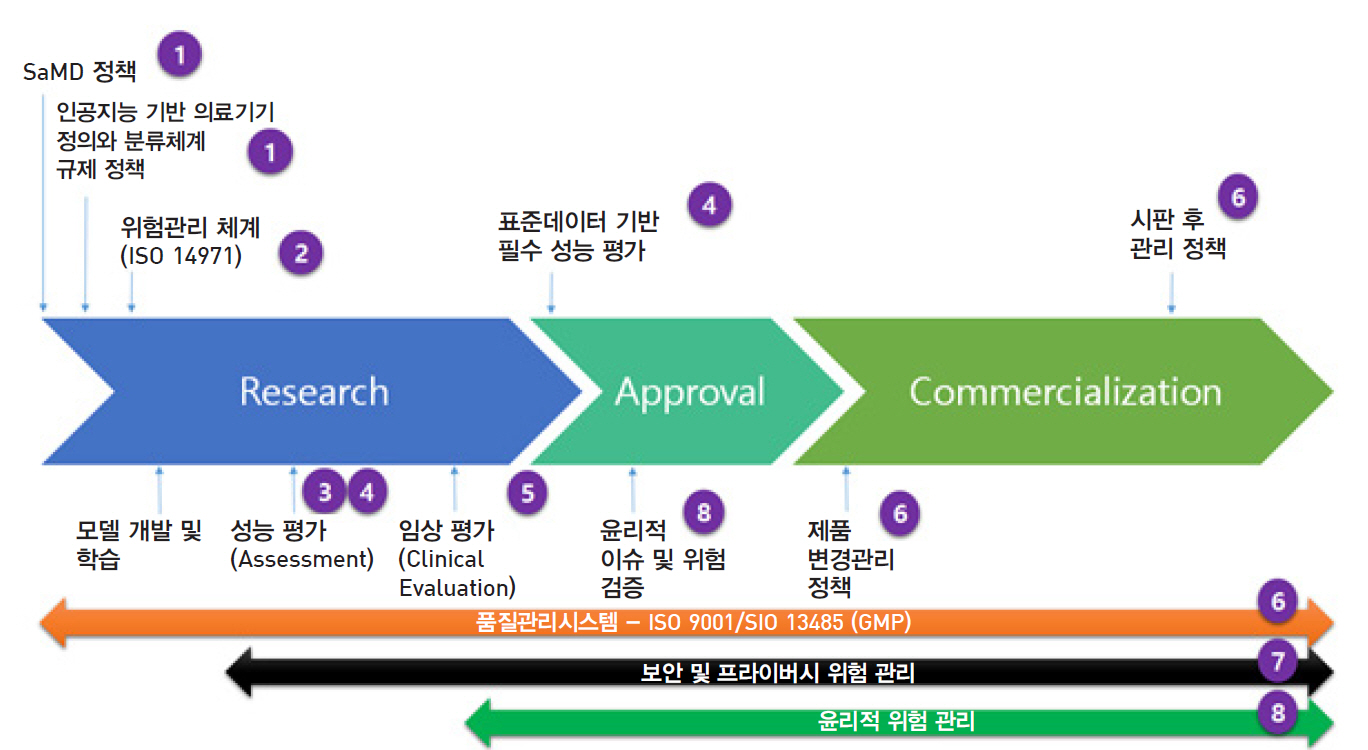
의료 인공지능의 대표적 응용 분야인 인공지능 기반 의료기기 개발과 상용화라는 전주기적 라이프 사이클 관점에서 보면 8가지 핵심 이슈들은 그림 4와 같이 연관되어 있음을 알 수 있다.
의료용 전기기기 분야에서는 인허가 필수 성능 및 안전 요구사항에 대한 기준 규격들이 대부분 IEC 60601 시리즈(또는 ISO 80601 시리즈) 국제 표준들과 연관되어 있는 것처럼, 인공지능 기반 의료기기 등의 시장이 확대될 경우, 국가별 기준 규격과 국제 표준화 연계, 그리고 국제 규제 간 조화 요구도 커질 것으로 예상된다.
그러나 현재 시점에서 볼 때 패러다임의 큰 전환이 필요한 상황-즉, H/W 중심인 의료용 전기기기 중심의 안전관리/위험관리 체계에서 S/W 중심의 인공지능 기반 의료기기 안전관리/위험관리 체계로의 전환-이기에 다음과 같은 어려움과 장애들이 있는 상태이다.
-
• H/W 중심에서 S/W 중심으로의 의료기기 위험관리/성능평가/인허가 체계 변경
-
• 기존 위험관리/성능평가 체계와 다른 방식이며, 네트워크/클라우드를 사용하며 지속적으로 진화하는 서비스형 환경을 어떻게 신속하게 인허가하며 적시에 관리할 수 있도록 할 것인가 문제
-
• SaMD 중심의 인공지능 기반 의료기기들에 대한 국제 표준화 담당 위원회 부재(현재 기존 의료용 전기기기 관련 국제 표준은 IEC TC62에서 개발하였으나, SW 중심 체계를 맡을 위원회가 부재)
-
• 인공지능 기반 의료기기가 이머징 기술이기에 국가별 기술격차로 인한 국제 조화의 어려움
-
• 관련 의료 ICT 융합 기술 전문가의 부재
앞으로 FDA, K-FDA, C-FDA 등에서도 이러한 이슈들을 해결하기 위해 다양한 새로운 규제 프레임워크들을 시도하고 있기에, 선행적인 글로벌 협력들을 추진하여 경험을 공유하며 공동 대응할 수 있는 중장기적 대책 방안 마련이 필요하다.
Ⅴ. 결론
최근 3년 동안의 인공지능 기술 분야의 발전은 놀라울 정도로 급속하게 이루어지고 있다. 각 국가별 정책적 지원도 전폭적으로 이루어지고 있고, 글로벌 다국적 기업들의 투자들도 전방위적으로 이루어지고 있다. 최근 소프트뱅크 손정의 회장이 “첫째도 AI, 둘째도 AI, 셋째도 AI”라고 말한 것처럼, 인공지능 기술에 대한 전략적 투자와 실행이 더욱더 중요한 상황이 되고 있다.
이러한 상황 속에서 특히 중국의 국가 전략을 중요하게 살펴볼 필요가 있다. 중국은 국무원이 17년 7월 발표한 ‘차세대 인공지능 발전규획’에서 2030년까지 세계 인공지능 강국으로 도약하기 위한 거시 로드맵을 제시하고, 17년 12월 공업정보화부에서 발표한 ‘차세대 인공지능 산업 발전 촉진 3년 행동계획’을 통해 상세 추진 전략을 제시하며, 전국가적인 차원에서 전방위적 투자와 실행을 단합된 모습으로 진행하고 있다[18,19].
특히 ‘차세대 인공지능 발전 규획’에서 인공지능 산업 확산을 위해 필수적인 요소로 인공지능 기술 표준 체계의 필요성을 언급하며, 이를 위해 기초 공통성, 상호 연결, 산업 응용, 인터넷 안전, 사생활 보호 등의 인공지능 기술 표준을 수립할 것을 선언하고 있다.
또한 ‘3개년 행동계획’에서는 중점 임무로 인공지능 제품 개발 촉진을 선언하고, 뇌, 폐, 눈, 뼈, 심혈관, 유방 등 질병 영역의 진단 기술을 개발하여 상품화하고 1% 미만의 false-negative rate와 5% 미만의 false-positive rate로 탐지하는 인공지능 기반 의료 영상 보조 진단 시스템 등을 2020년까지 개발하는 목표를 제시하기도 했다.
그리고 이러한 품질 확보를 위해 2020년까지 행동 목표로 인공지능산업지원시스템을 기본적으로 구축하고 일정 규모의 고품질 라벨 데이터자원베이스, 표준측정데이터베이스의 구축 및 오픈, 인공지능표준시스템, 분석평가시스템 및 안전보장시스템 틀을 기본적으로 구축하여 산업발전환경을 개선한다는 목표도 설정하였다[19].
현재 중국에서는 이러한 전략적 투자와 집중에 힘입어 다양한 의료 인공지능 기술과 서비스들이 폭발적으로 성장하고 있다. 예를 들어, 설치비용 500만 원밖에 안 되는 3m2 정도 넓이의 ‘무인 진찰실’에서 혈압과 체온을 재고 영상의 인공지능(AI)의사에게 증상을 얘기하면, 잠시 후 이를 기초로 원격지 의사가 추가 질문을 건넨 뒤 복용 약을 추천하는 ‘1분 진료소’도 설치되고 있다.
미국에서 허가된 의료 인공지능 제품과 서비스가 40여 종 이상 등장하였고, 국내에서도 뷰노, 루닛, JLK 등에서 10종 이상이 허가된 것처럼 앞으로 의료 인공지능 기반 응용과 서비스는 더더욱 빠르게 확산될 것이다. 이러한 시장 요구를 반영하여 FDA가 보다 신속한 의료 인공지능 제품 인허가 체계[17]를 만들기 위해 다양한 고민을 하는 것처럼, 국내에서도 의료 인공지능 산업 활성화에 필요한 표준과 허가 기준, 국제 조화와 규제 체계와 정책들도 빠르게 재조정되어야 하는 상황이다.
결국 중국의 인공지능 육성 계획 사례에서 보듯 표준화는 지속 성장을 위해 필요한 핵심 기반이며 필수적으로 뒷받침되어야 하는 요소이다. 국내에서도 앞으로 의료 인공지능 기술의 혁신과 확산이 가능하도록 하기 위해서는 거시적이고 중장기적 관점에서 표준 기반 체계를 근간으로 하는 국가적 전략과 체계적인 정책적 지원, 산업 활성화, 그리고 협력이 전략적으로 뒷받침되어야 할 것이다.
약어 정리
AI
Artificial Intelligence
AHG
Ad-hoc Group
AUC
Area Under the Curve
CT
Clinical Terms
FDA
Food and Drug Administration
FG
Focus Group
GDPR
General Data Protection Regulation
HPO
Human Phenotype Ontology
ICD
International Classification of Diseases
ICHI
International Classification of Health Interventions
IEC
International Electrotechnical Commission
IMDRF
International Medical Device Regulators Forum
ISO
International Organization for Standardization
ITU
International Telecommunication Union
JTC
Joint Technical Committee
ROC
Receiver Operating Characteristic
SaMD
Software As Medical Device
SC
Sub Committee
SNOMED
Systematized Nomenclature of Medicine
WG
Working Group
WHO
World Health Organization
참고문헌
그림 1
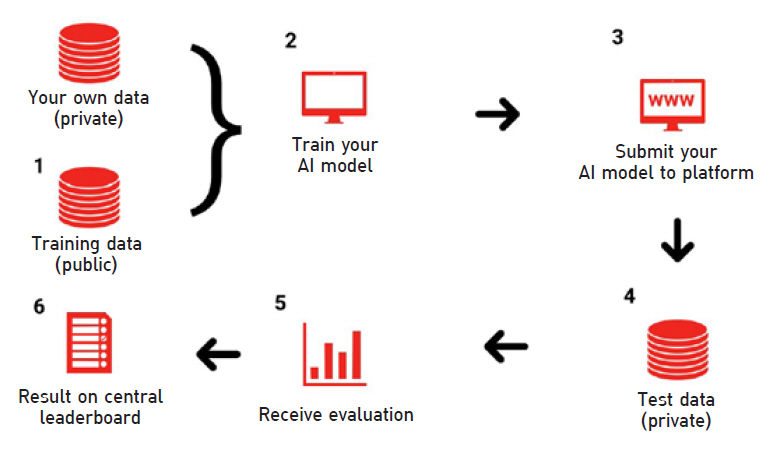
벤치마킹 모델
그림 2
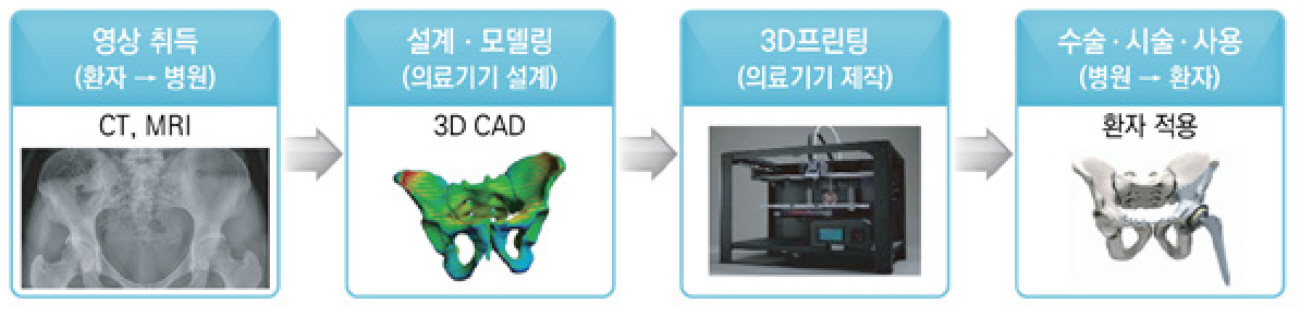
의료 3D 프린팅 제작 단계
그림 3
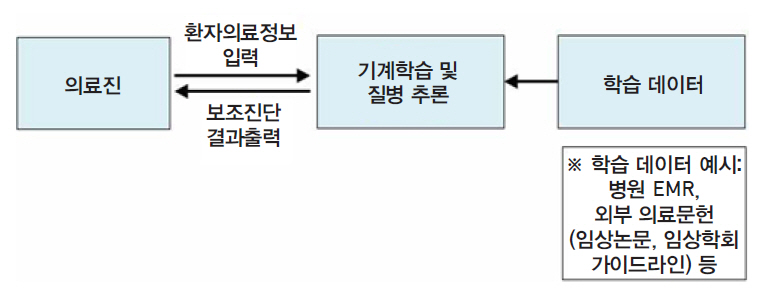
기계학습 방식의 인공지능 기반 의료기기 제품특성
그림 4
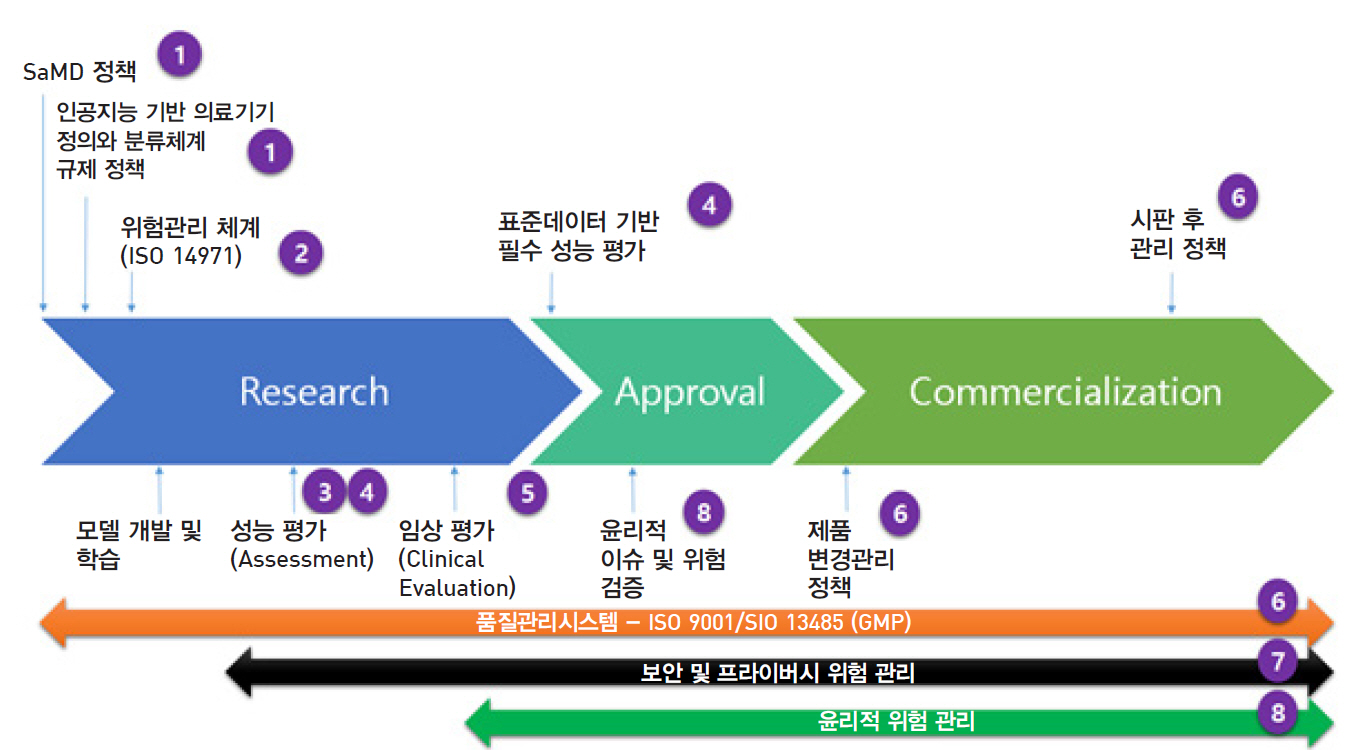
핵심 정책/표준화 이슈와 인공지능 기반 의료기기 생애 주기 연관도