전자약 연구개발 동향
R&D Trends in Bioelectronic Medicines
- 저자
-
김용희뇌휴먼인터페이스연구실 josephinkim@etri.re.kr 정상돈뇌휴먼인터페이스연구실 jungpol@etri.re.kr 이성규지능형센서연구실 Hermann@etri.re.kr 김혜진지능형센서연구실 nolawara@etri.re.kr 변춘원실감디스플레이연구실 cwbyun@etri.re.kr 이정익실감소자원천연구본부 jiklee@etri.re.kr 송기봉미래원천연구본부 kbsong@etri.re.kr 강성원ICT창의연구소 kangsw@etri.re.kr
- 권호
- 35권 3호 (통권 183)
- 논문구분
- 일반논문
- 페이지
- 98-110
- 발행일자
- 2020.06.01
- DOI
- 10.22648/ETRI.2020.J.350310
 본 저작물은 공공누리 제4유형: 출처표시 + 상업적이용금지 + 변경금지 조건에 따라 이용할 수 있습니다.
본 저작물은 공공누리 제4유형: 출처표시 + 상업적이용금지 + 변경금지 조건에 따라 이용할 수 있습니다.- 초록
- Precise detection and modulation of electrical signal patterns passing through peripheral nerves connecting organs and brainstems, referred to as electroceuticals or bioelectronic medicines, have emerged as a new type of treatments for neural disorders and chronic diseases. With the rapid advancements in neural interface technologies, electroceuticals are the focus of treatments for these disorders or diseases. In this paper, we introduced electroceuticals as an extension of neuromodulation for the treatment of chronic diseases, such as diabetes, rheumatoid arthritis, obesity, and bladder dysfunction, without side effects that are unavoidably elicited when conventional drugs are taken. Further, this paper reviewed the anatomy of the peripheral nervous system, treatment examples for chronic diseases, technological demands for peripheral nerve interfacing, global R&D programs and market trends for electroceuticals, and prospects on electroceuticals.
Share
Ⅰ. 서론
신체에서 일어나는 신진대사 대부분은 복잡한 화학반응에 의해서 이루어진다. 기존 화학적 성분 기반 약물(Drug)을 이용한 전통적인 신체 대사기능 조절(그림 1(b))은 수많은 질병치료에 중요한 역할을 해 오고 있으나, 약이나 주사약 등은 혈관을 통해 전신으로 공급되기 때문에 질병치료 효과 외에 부작용이 수반되는 문제가 있다. 실제 미국에서는 질병치료를 위해 복용하는 약물로 인한 부작용이 매년 200만 건 이상 보고되고 있으며, 약물 부작용으로 인한 사망은 폐질환, 당뇨, 자동차 사고에 이어 사망원인 4번째를 차지하고 있다[1]. 약물 부작용에 대한 심각성이 사회적 이슈로 대두되면서 약물치료를 대체할 수 있는 방법들에 대해 많은 연구개발이 시도되고 있다[2].
그림 1
(a) 신경자극에 의해 대사조절이 가능한 장기 (b) 약물치료에 의한 대사조절 (c) 전기자극에 의한 질환치료 (d) 줄기세포 등 인공조직 대체
출처 Reprinted from B. J. Seicol et al., “Neuromodulation of metabolic functions: from pharmaceuticals to bioelectronics to biocircuits,” J. Biol. Eng., Vol. 13, 2019, 67:1-12. CC BY 4.0.
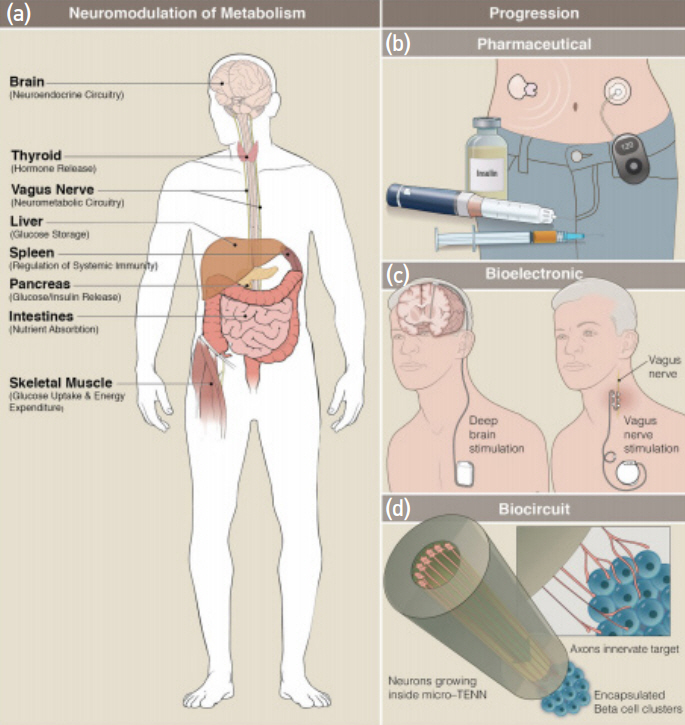
인체에서 진행되는 신진대사는 생존을 위한 필수적인 기능으로 체내 장기에서 일어나는 여러 생리학적 시스템들의 협력 활동을 필요로 하며, 이와 같은 작용으로 신체의 항상성이 유지된다. 음식 섭취, 기온 변화, 에너지 소모, 감염 등 외부자극에 대한 신체 항상성 유지는 내분비계와 신경계에 의해 이루어진다. 예를 들어, 사이토킨(Cytokine)은 주로 염증 등 면역기능의 변화를 유발하는 면역세포에 의해 생성되고 분비되는 신호 단백질인데, 이의 생성과 분비는 신경회로에 의해 조절되는 대사기능 가운데 하나이다. 부분적인 장기의 손상이나 기능손실 그리고 신경회로의 오작동에 의해 면역기능 등을 포함하는 대사과정이 비정상 상태가 되면 질병 또는 질환이 생겨난다[3]. 근래 기존의 화학적 약을 기반으로 신경신호를 제어하는 방법과는 달리 전기자극 등을 통해서 신경신호를 인위적으로 제어하여 면역 및 대사 관련 질환을 치료 또는 완화하는 약물 대체 치료법이 등장하였는데, 이를 전자약(Electroceuticals) 또는 바이오전자 의료(Bioelectronic medicine)로 부르고 있다[4]. 전자약은 약물 대신 전기, 빛, 초음파 등을 이용하여 신경회로를 자극하여 대사기능을 조절함으로써 신체의 항상성을 회복 또는 유지시키는 치료법으로 정의될 수 있다[4-7].
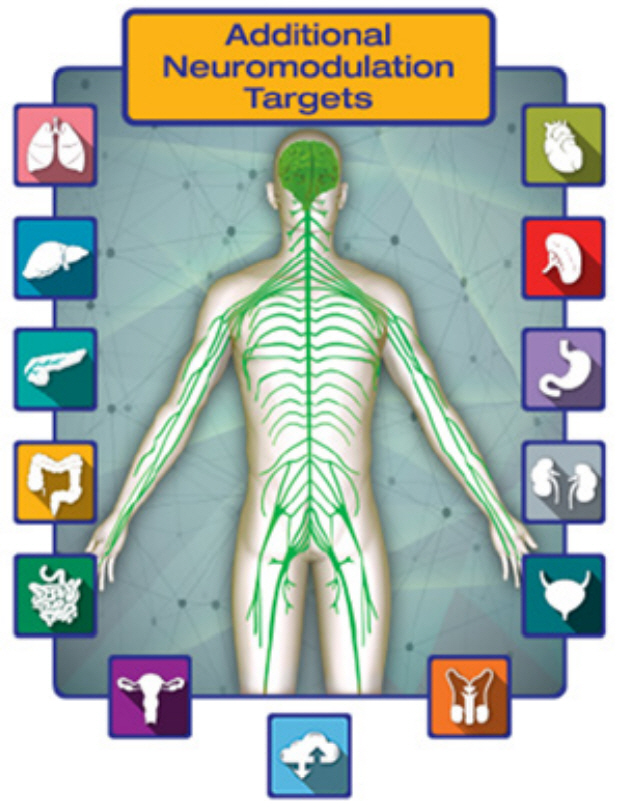
신경계는 뇌와 척추를 포함하며 체내 대사 상태를 전체적으로 감지하고 감지 결과에 따라 적절한 내분비 신경신호를 방출함으로써 대사를 조절하는 중추신경계, 그리고 중추신경계에서 파생되어 온몸에 가지처럼 분포하며 방출된 신경신호를 장기에 전달하는 말초신경계로 구성된다[3]. 중추신경계인 뇌신경계의 기능이 손상되는 경우 뇌졸중, 우울증, 간질, 파킨슨병과 같은 다양한 신경질환이 발생되는데, 인공적인 신경자극으로 손상된 기능을 대체하는 것이 가능하다. 이러한 치료법은 신경조절(Neuromodulation)이라고 불리는데, 일부 효과가 검증되어 현재 DBS(Deep Brain Stimulation) 등이 FDA 승인되어 시술되고 있다(그림 1(c) 왼쪽)[8,9]. 하지만, 이와 같은 심각한 뇌 질환과 전신 마비를 제외하면 신체 대사, 감각, 운동 기능에 관여하는 뇌 영역에 신경 전극을 삽입하고 자극하는 것에 대해서, 특히 정신 상태가 온전한 경우, 심리적 거부감이 해당 기술의 보급에 큰 걸림돌이 되고 있다. 말초신경계의 핵심신경 가운데 하나인 미주신경(Vagus nerve)은 갈색지방조직, 간, 췌장 등 신체의 핵심 장기와 연결되어 있다(그림 1(a))[10-12]. 장기와 뇌를 연결하는 말초신경계를 인공적으로 자극하는 신경조절법은 뇌신경 자극에 비하여 거부감이 상대적으로 낮은 장점이 있어 말초신경 자극을 통한 신경조절 분야에서의 전자약 기술 적용이 좀 더 유망하다(그림 1(c)).
본 고에서는 말초신경 인터페이스를 통한 대사조절을 기반으로 하는 전자약 방법이 유효한 만성질환 완화와 치료에 대한 소개, 성공적 적용을 위한 요소기술들과 관련 기술들의 연구개발 동향 및 향후 발전 전망, 그리고 주요 글로벌 연구개발 프로그램과 시장 전망, 그리고 향후 발전 전망을 기술하고자 한다.
Ⅱ. 전자약 치료법
1. 말초신경계
말초신경계는 신경계에서 중추신경계를 제외한 나머지 신경계를 통칭하며, 그림 2(a)와 같이 중추신경계에서 나온 신경이 몸의 각 구석까지 뻗어 있어서 장기, 피부와 팔다리의 신경을 중추신경계와 연결해 주는 역할을 한다. 말초신경계는 뇌와 척수에 정보를 전달하는 구심성 신경(Afferent nerve)과 뇌와 척수의 정보를 장기 또는 근육에 전달하는 원심성 신경(Efferent nerve)으로 구분된다. 또한 말초신경계는 기능적으로 체세포신경계(Somatic nervous system)와 자율신경계(Autonomic nervous system)로 분류되는데, 체세포신경계는 획득한 감각 정보를 뇌와 척수에 전달하고, 뇌와 척수에서 전달받은 운동명령을 근육신경섬유에 전달하는 역할을 한다. 이러한 체세포신경계를 통해 전달되는 신경신호는 인공 팔 제어와 인공감각 감지에 활용 가능하다. 자율신경계는 내장 반사신경(Visceral reflexes)을 조절하고 혈압, 체온, 대사 등과 같은 핵심적인 생물학적 프로세스 등을 조절하여 인체가 항상성을 유지하도록 하는 역할을 하며, 교감신경(Sympathetic nerve)과 부교감신경(Parasympathetic nerve)으로 세분된다. 교감신경은 환경변화에 따른 잠재적 위험에 대처할 수 있도록 심박수, 호흡, 근육의 혈류량, 땀 분비량, 동공 크기 등을 조절하는 역할을 한다. 부교감신경계는 잠재적인 위험상황에서 벗어나면 심박 수와 호흡을 늦추며 혈류를 줄이고, 동공을 수축시키는 등의 역할을 하여 정상적인 신체기능을 유지할 수 있도록 조절하는 역할을 한다[13-16]. 말초신경은 또한 뇌와 내장을 연결하는 역할을 하는데, 내장의 정보를 뇌로 전달하는 구심성 말초신경 자극을 통해서 불안장애를 조정하는 것이 가능하다[17].
그림 2
(a) 휴먼 신경계와 (b) 말초신경-장기 연결도
출처 (a) 게티이미지뱅크, 무단 전재 및 재배포 금지, (b) BruceBlaus, "Medical gallery of Blausen Medical 2014," WikiJournal of Medicine 1 (2). DOI:10.15347/wjm/2014.010 CC BY 3.0.
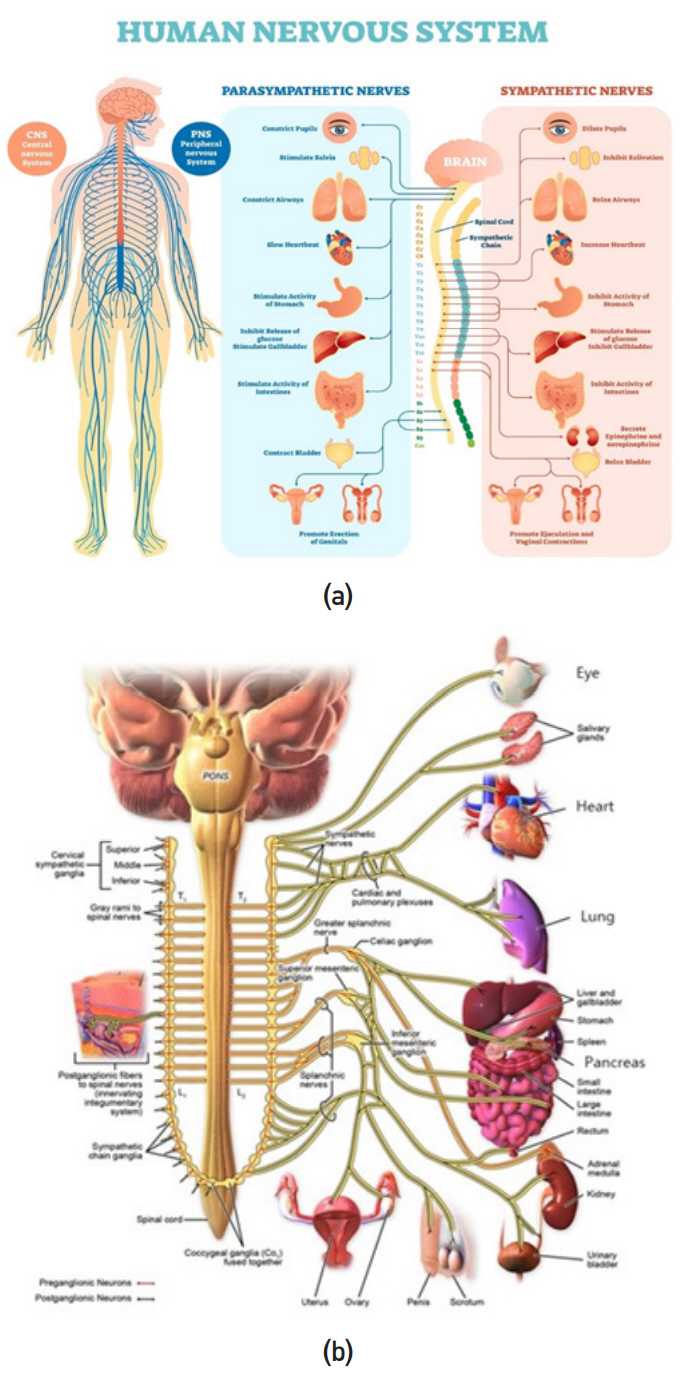
신체에는 수많은 말초신경들이 분포하는데 자율신경계에서 신체 대사에 가장 많이 관여하는 말초신경은 미주신경이다[18,19]. 미주신경은 그림 2(b)와 같이 각 장기별로 개별적인 연결성을 가지고 있으며, 장기 제어는 스파이크 형태의 활동전위 패턴에 의해 이루어진다. 활동전위 패턴은 신경전달물질의 양을 제어하며, 이를 통해 세포 내 신호전달물질 등을 활성화하여 연결된 세포 또는 주변세포의 활동에 영향을 주게 된다. 전자약을 통한 신경제어방법은 미주신경에 전극과 제어장치를 삽입하고 인위적인 신경 활동전위 조절을 통해 신경전달물질의 활성화를 제어하는 방법이다. 이를 통해서 항상성을 잃은 신체 대사의 기능을 회복시키는 역할을 하게 된다. 미주신경 이외에 엉치신경(Sacral nerve) 자극을 이용한 변실금 및 위장장애 치료법이 연구되고 있다[20].
2. 전자약 적용예시
말초신경자극은 대표적 대사질환인 당뇨병, 자가 면역질환인 류마티스, 전 세계적 주 사망원인 가운데 하나인 심혈관 질환, 비만, 요실금이나 방광장애와 같은 배뇨장애, 천식, 우울증, 간질, 통증 등 다양한 질환에 적용되고 있다. 이 가운데 간질에 의한 발작 치료를 목적으로 하는 미주신경 자극기는 1997년에[21], 우울증 치료를 위한 미주신경 자극기는 2005년에[11], 그리고 미주신경의 가지인 등의위(Dorsal gastric)를 자극하는 비만치료용 자극기는 2015년에[22] 각각 FDA 승인이 되었다. 또한, 요실금 치료를 위한 Medtronic의 INTERSTIM은 2011년에 승인되어 척추뿌리(Spinal cord root) 부분에 시술되고 있다[23]. 현재까지 FDA 승인된 전자약은 말초신경 자극을 기반으로 하는 뇌신경조절과 심장, 위, 방광과 같은 장기에 존재하는 신경을 직접 자극하는 방법이 주류를 이루고 있으며, 최근에는 장기에 존재하는 신경 대신에 미주신경과 같은 말초신경을 자극하거나 당뇨병 및 류마티스 등과 같은 대사 및 내분비 관련 질환에 대한 전자약 적용이 연구단계에 있다. 연구단계에 있는 말초신경자극 기반 전자약 적용 사례는 다음과 같다.
가. 류마티스 관절염
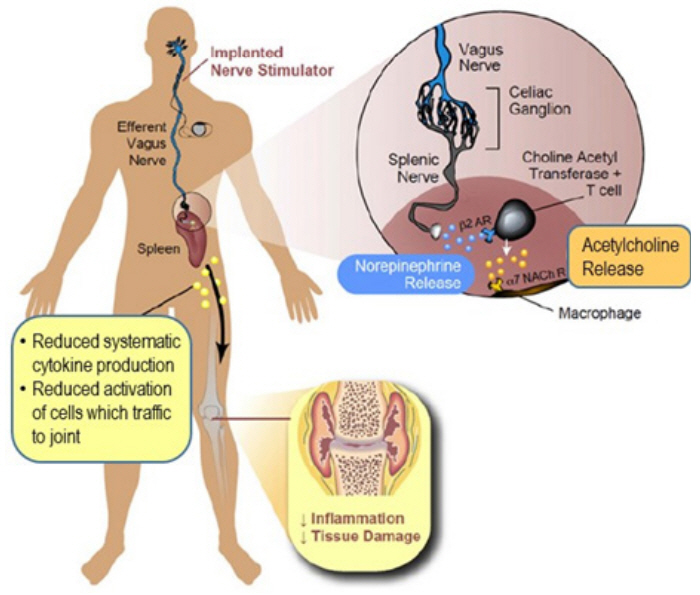
류마티스 관절염은 관절부위에 발생하는 자가면역질환의 하나로서 관절의 활막에서 발생하는 염증반응이며, 활막염은 관절표면 조직을 연하게 하고 부식시켜 관절이 제 기능을 하지 못하게 한다. 관절염을 가지고 있는 대부분의 환자들은 약물을 복용하여 통증을 완화시키는데 약물로 인한 부작용이 심각하다. 미주신경은 체내 염증을 감지하고 조절하는 데 중요한 역할을 하는데, 미주신경 자극법의 메커니즘은 약물을 복용하여 염증성 물질인 사이토킨 생성을 억제하는 것과 같은 원리이다. 2000년 Tracey 등은 쥐를 대상으로 한 연구에서 미주신경 자극을 통해 관절염증을 상당히 감소시킬 수 있음을 보고하였으며[24], 2016년 임상시험에서도 동일한 결과를 얻었음을 발표하였다[25]. 미주신경을 자극하면 신경전달물질인 아세틸콜린이 생성되며, 생성된 아세틸콜린은 사이토킨을 분비하는 세포에 작용함으로써 염증성 물질인 사이토킨 분비를 억제하여 관절염과 이에 수반되는 통증을 완화시킬 수 있다(그림 3).
그림 3
미주신경 자극을 통한 류마티스 관절염 치료 메커니즘
출처 F.A. Koopman et al., “Vagus nerve stimulation: A new bioelectronics approach to treat rheumatoid arthritis?” Best Practice Res. Clinical Rheumatology, vol. 28, no. 4, 2014, pp. 625-635, CC BY-NC-ND 3.0.
나. 당뇨병
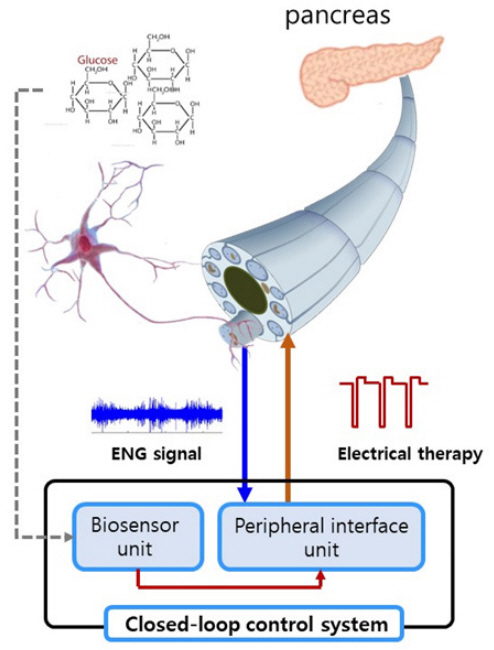
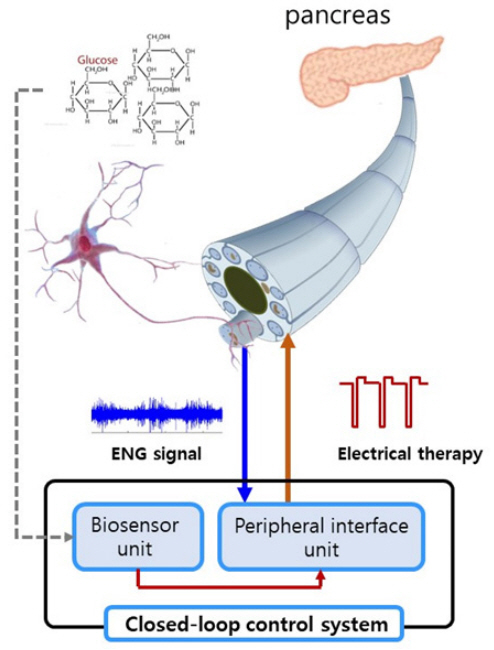
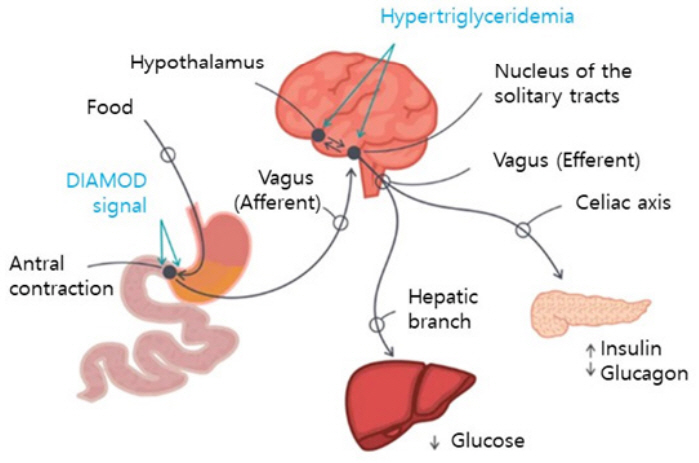
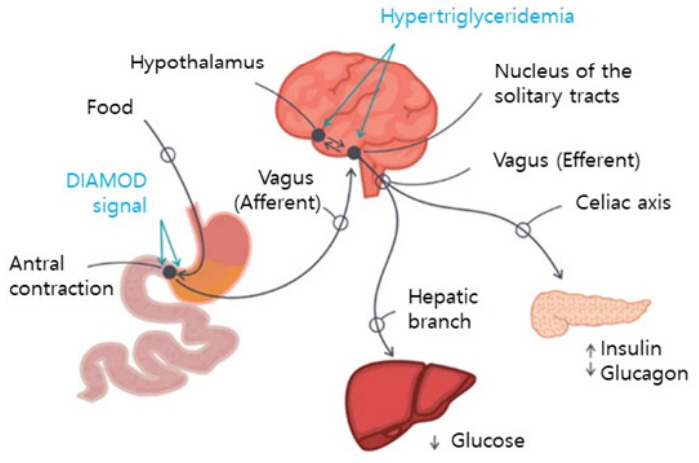
당뇨병은 혈액 내 포도당이 상승하는 만성대사질환으로 세계에서 4억 명 이상이 당뇨로 인한 질환을 가지고 있으며, 2030년에는 당뇨 및 합병증으로 인한 사망이 사망원인 7번째를 차지할 것이라고 예측되고 있다[26]. 제1형 및 제2형 당뇨병은 각각 췌장 β-세포의 파괴로 인슐린 분비가 제한되는 자가면역성 질환과 인슐린 작용의 결함에 의한 질환으로 모두 만성과 고혈당증을 특징으로 한다. 근래, 혈당을 효율적으로 줄이기 위하여 포도당 감지-인슐린 공급으로 구성된 폐-루프 인공췌장이 개발되었는데[27], 전자약은 인슐린 공급 없이 전기 자극으로 인슐린 분비가 가능하다. 구강, 내장, 그리고 간문맥 정맥(Hepatoportal vein)에 존재하는 포도당 감지 세포들로부터 포도당 정보를 제공받은 뇌간(Brainstem)과 시상하부(Hyperthalamus)는 포도당 항상성 유지를 위하여 미주신경을 통해 포도당을 생성하는 간과 호르몬을 분비하는 내분비 췌장을 제어한다(그림 4). 예를 들면 췌장에 연결된 미주신경 말단은 아세틸콜린을 분비하며, 췌장의 β-세포는 이에 반응하여 인슐린을 분비하게 된다[28,29]. 미주신경은 인슐린 분비뿐만 아니라 β-세포의 증식과 인슐린 감도를 제어하는 것으로 알려져 있다. 아직까지 미주신경 신호와 인슐린 분비 간의 정확한 상관관계는 정립되어 있지 않은데, 인공적 미주신경 자극의 효용성 향상을 위해 해결해야 할 핵심 문제로 남아 있다[29].
그림 4
미주신경 자극에 의한 혈당조절 메커니즘
출처 https://bigthink.com/philip-perry/darpa-is-investing-in-a-platform-that-accelerates-learning
다. 비만
비만은 미국 성인의 거의 40%에 영향을 끼치며 암, 심혈관 질환 및 당뇨병을 포함한 높은 수준의 동반 질환과 깊은 연관이 있다[30,31]. 복부신경에 가하는 전기 자극만으로 음식섭취와 체중을 감소시킬 수 있지만, 미주신경을 자극하면 구토 경로를 자극하여 음식을 섭취하는 것과 같은 혼동을 유발할 수 있다. 또한 인슐린, 글루카곤, 위산 분비를 포함한 신진대사와 음식물 소화과정을 조절할 수 있는 미주신경 자극 유도반응이 존재하는 것으로 알려져 있으며, 이를 비만 치료에 적용하는 것이 시도되었다[32].
라. 방광기능장애
방광기능 장애는 심장병이나 당뇨병보다 사망에 이를 확률이 낮지만, 요실금 관련 문제는 많은 인구에 영향을 미치고 있으며 여성들 중 17%가 요실금이나 배뇨 장애로 불편을 겪고 있다. 미국에서는 매년 600억 달러가 넘는 비용이 배뇨 장애 치료에 지출되고 있다[33]. 척추를 자극하여 요실금을 치료하기 위한 자극기는 이미 2011년에 FDA 승인되었으며, 말초신경 자극을 통한 배뇨 기능의 제어 가능성도 동물 실험 등을 통하여 확인된 바 있다. 이 연구에서 미주신경의 구심성 신경을 자극한 결과 자극 빈도에 따라 방광의 반응이 다름을 확인하였고, 불규칙적인 주파수를 가하였을 때 방광 기능이 활성화되는 것을 확인하였다. 이 결과로부터 척 추자극뿐만 아니라 말초신경 자극을 통한 배뇨기능 개선 가능성이 확인되었다[34].
III. 말초신경인터페이스 기술개발동향
1. 기술적 요구사항
전자약이 성공적으로 개발되고 보급되기 위해서는 목표로 하는 신경을 선택적으로 자극할 수 있고 신호를 측정할 수 있는 초소형 신경전극, 초소형 신경신호 처리 및 자극기, 무선통신 및 충전, 폐-루프(Closed-loop) 제어용 센서 등을 필요로 하는데(그림 5), 이를 요구 성능으로 분류하면 다음과 같이 정리될 수 있다.
가. 감도 및 자극 효율(Sensitivity & Stimulation efficiency)
검출 신호가 아닌 기타 잡음으로부터 분리된 신경 신호를 정확히 측정하기 위해서는 신경 전극의 신호 대비 잡음 비 향상이 요구되며, 이를 위한 전극의 임피던스 제어 기술 개발이 필요하다. 그리고 신경조절을 위해 전기 자극하는 경우, 신경조직의 손상을 최소화하기 위하여 신경전극의 전하주입한계와 전하주입효율 향상 기술 개발이 필요하다.
나. 선택도(Selectivity)
오동작 없는 제어를 위해서는 말초신경에서 자극이 가해질 표적신경 선택 그리고 적합한 자극패턴과 자극 기간 등에 관한 정보가 요구된다. 신경을 구성하는 축삭(Axon)의 직경이 0.25~25μm로 매우 작고, 그 수가 미주신경의 경우 약 100,000개나 되며, 불규칙적으로 배열되어 있기 때문에 표적신경의 선택은 매우 어려운 작업이다. 또한, 말초신경은 다수의 장기와 연결되어 있고 장기와 중추신경계 방향으로 구분되어 있기 때문에 잘못된 선택은 오동작을 초래할 수 있다. 단일 프로브에서 개별 전극의 수가 많아지면 전극의 조합을 다중으로 구성하여 표적 선택을 향상시킬 수 있다. 반면에 개별 전극의 수가 증가할수록 전극 수술의 난이도가 높아지고, 제어기에서는 각 전극별 고유한 자극 진폭, 펄스 지속시간, 부하 시간율(Duty cycle), 자극 주파수 등의 자극 변수들이 기하급수적으로 증가하기 때문에 최적의 자극 매개변수 선정과 실시간 폐-루프 제어에 있어서 기계학습 접근법이 필요하다.
다. 반응도(Responsiveness)
말초신경의 신경절(Ganglia) 또는 축삭의 자극 효과를 정량화할 수 있는 대사물질 그리고 신경화학 방출 또는 면역반응의 마커를 측정하기 위한 화학센서, 그리고 장기의 움직임이나 방광 압 등을 측정할 수 있는 물리센서가 요구된다.
라. 수용도(Acceptance)
시술 환자에 거부감을 최소화할 수 있도록 고 신뢰성 말초신경인터페이스, 저전력 프로세서 및 회로부품, 무선 충전, 무선 통신, 생체적합 패키징 등의 기능을 포함하는 삽입형 시스템이 요구된다.
마. 자가 조절(Self-control)
표적 기능을 꾸준히 수행할 수 있도록 감지하고 그 결과에 따른 자극과 자극 후의 신경조절이 외부의 관여 없이 독립적으로 수행할 수 있는 지능형 폐-루프 제어시스템 개발이 요구된다.
2. 말초신경 전극 기술동향
말초신경전극은 주로 바이오닉 보철 팔 제어[35]와 촉각 등 인공감각 인지[36,37]를 위한 인터페이스용으로 개발되었는데, 최근 전자약 목적으로 적용되고 있으며, 새로운 구조와 기능을 가진 전극들이 개발되고 있다. 말초신경전극은 그 개발 역사가 길지만 상용화는 아직까지 제한적이며, 표준적인 시술 방법이 마련되지 못하고 임상 적용에 따른 실패 요인 등에 대한 평가가 축적되고 있는 단계에 있다[38]. GSK는 선택도가 현저하게 향상된 말초신경전극을 개발하고 있으나 아직까지 공개하지 않고 있다.
말초신경전극은 삽입형과 비삽입형으로 가장 크게 분류되는데, 삽입형의 경우 그림 6(a)와 같은 신경다발에 적용되는 위치에 따라 표면전극, 관통전극, 재생전극으로 구분된다. 본 고에서는 열거된 삽입형 전극과 비삽입형 전극인 경피신경전극에 대해 간략하게 살펴보았다. 보다 상세한 말초신경 인터페이스 기술은 초음파 및 광 자극 기술 등과 함께 후속 편에서 다룰 예정이다.
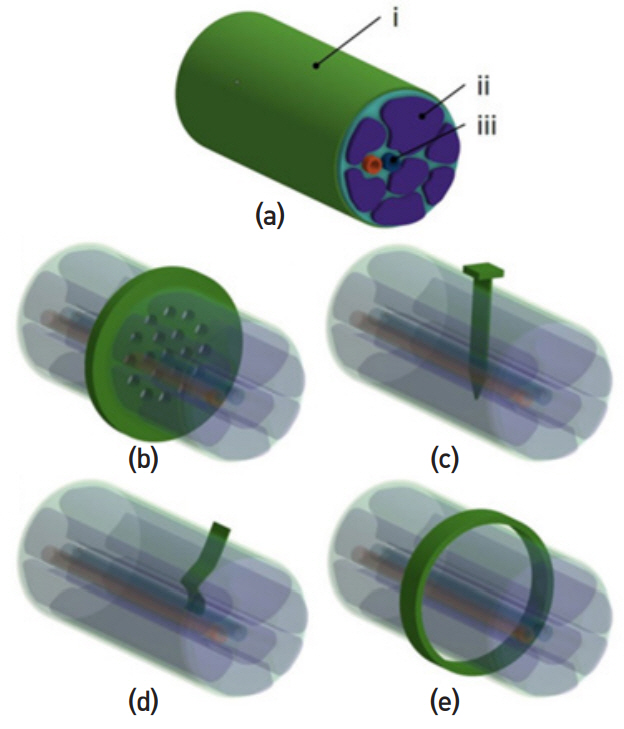
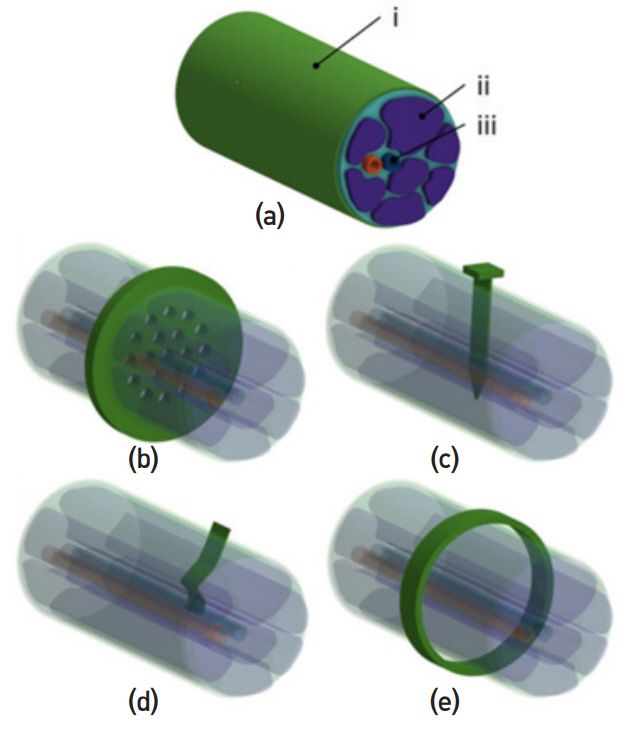
그림 6
삽입형 말초신경전극 (a) i) 신경상막(epineurium), ii) 축삭을 내포하는 섬유속, iii) 혈관 (b) 재생전극 (c, d) 관통전극 (e) 표면전극
출처 Reprinted from C. Russell et al., “Peripheral nerve bionic interface: a review of electrodes,” IJIRA, vol. 3, 2019, pp. 11-18, CC BY 4.0.
가. 표면전극(Surface electrode)
cuff 전극으로 대표되는 표면 전극은 신경다발을 감싸는 형태로 불연속적인 신경다발을 직접적으로 제어할 수 있다. 그림 6(e)와 같은 형태의 cuff 전극은 개별 전극 면이 안쪽에 위치하고 있으나, 신경과 전극 사이에는 신경외막이 존재하여 일종의 절연막과 같은 역할을 함으로써 신경신호의 세기와 전기 자극 효과가 감소될 수 있다. 표면전극의 또 다른 형태의 전극으로는 FINE 전극이 있다. FINE 전극은 평평한 형태의 cuff 전극으로 신경을 눌러주도록 설계되어 신경다발이 근막과 분리될 수 있으며, 결과적으로 자극과 기록의 선택성이 증가된다. cuff와 FINE 전극을 보완하기 위한 방법으로 신경에 좀 더 밀접하게 접근할 수 있도록 설계된 분할 링(Split ring) 형태의 전극을 이용한 자극 시도도 최근에 이루어지고 있다. 전체적으로 표면전극은 전극이 신경과 직접 접촉하지 않기 때문에 특정 신경을 자극하거나 특정 신경의 신호를 기록할 수 없는 단점을 가지고 있다. cuff 전극은 약 10년 정도의 삽입 내구성을 가지는 것으로 보고되었다.
나. 관통전극(Penetrating electrode)
관통전극은 전극이 신경다발을 관통하여 삽입되는 전극으로 전극의 삽입 위치에 따라 LIFE(그림 6(c))와 TIME(그림 6(d)) 두 종류가 있다. LIFE 전극은 유연한 절연체로 보호된 와이어 형태의 전극이며, 신경다발에 접촉되는 전극이 노출된 형태를 가지고 있다. 이 전극은 신경다발과 같은 축으로 삽입되고 양쪽 끝은 바깥쪽으로 노출된다. 피복된 직경 25~50μm의 Pt 또는 Pt-Ir 와이어가 주로 사용되며, 신경다발에 접촉되는 신경전극은 0.5~1mm 정도 노출되어 있다. LIFE 전극은 삽입 3개월 후 경미하고 가역적인 손상을 보이는 것으로 알려져 있다. TIME 전극은 여러 개의 전극이 신경다발 축에 수직으로 관통하여 삽입되도록 설계되어 여러 개의 신경다발과 접할 가능성이 크기 때문에 공간 선택성이 우수한 장점을 가지고 있다.
다. 재생전극(Regenerative electrode)
재생전극(그림 6(b))은 절단된 신경 사이에 위치하여 신경 재생 기능을 포함하는 전극으로 대표적으로 체 전극(Sieve electrode)과 재생 MEA가 있다. 체 전극은 전도성 물질로 이루어진 미세한 다공성 구조로 구성되어 있으며, 공간 분해능은 미세구멍의 크기에 의해 정해진다. 신경섬유는 전극의 미세구멍을 관통하여 자라나면서 절단된 신경이 이어지고 재생이 이루어진다. 재생 MEA는 신경 재생을 촉진하기 위하여 다공 내에 자극용 전극이 배열된 구조의 전극이다. 재생 MEA 삽입 후 28일 시점부터 3개월 동안 2.9±0.6개의 뉴런을 구별할 수 있었다는 동물실험 결과가 보고되었으나[39], 그 후 실제 임상 적용 사례는 보고되지 않고 있다. 재생전극은 선택도가 매우 높지만 절단된 신경에만 적용이 가능한 단점이 있다.
라. 경피신경전극(Transcutaneous electrode)
경피신경자극, 즉 피부를 통과해 신경을 자극하는 기술은 시술을 필요로 하지 않기 때문에 거부감이 거의 없이 안전하게 치료에 적용할 수 있는 장점이 있다. 2019년 FDA 승인된 안면 근육통 경감을 위한 휴대용 마이크로 전류 자극기를 예로 들 수 있다[40].
Ⅳ. 주요 연구개발 프로젝트
전통적인 약이 아닌 전자약 개발에 제약업체들도 참여하고 있는데, Johnson & Johnson과 GSK가 가장 적극적으로 참여하고 있다. 2013년 GSK는 전기 자극을 사용하여 신체의 신경회로를 조절함으로써 질병을 치료할 수 있는 치료의 새로운 개념으로 전자약에 관한 내용을 네이처(Nature)에 발표하였으며[5], 2014년에는 성공적인 전자약 개발을 위한 연구개발 로드맵을 발표하였다[41]. 그리고 2016년에는 Verily와 협력하여 전자약 전문 기업인 Galvani Bioelectronics를 설립하였으며, 7억 5천만 달러를 투자하고 있다. 2023년 류마티스 관절염 치료를 위한 전자약 출시를 목표로 하고 있다. GSK의 전자약 개념정리 및 로드맵 발표와 연계하여 대형 프로젝트들이 진행되었는데, NIH는 신체 장기-말초신경 연결지도의 제작과 신경신호 측정과 자극을 장기간 안정적으로 수행할 수 있는 말초신경전극 개발에 도움을 주는 것을 목표로 SPARC 프로그램을 진행하였다(그림 7)[42]. 특정 신경섬유를 표적할 수 있는 기술의 향상과 동시에 자극 효과에 대한 정확한 이해가 전자약에 필수적인데, SPARC 프로젝트에서는 전극을 삽입할 때 표적으로 하는 신경 또는 뉴런이나 그 사이의 시냅스를 최적으로 맞출 수 있는 전극 배열이 도출되도록 말초신경 연결지도 작성을 위한 데이터 수집을 진행하고 있다. 2016년 시작되었고 7년 동안 2억 4천만 달러가 투입되는 SPARC 프로젝트를 통하여 NIH는 각 장기로 들어가고 장기에서 나오는 수많은 신호를 분류하고, 이러한 신호를 이용하여 부작용 없는 전자약 치료법을 개발하고 있다. DARPA에서는 처치시간의 단축을 목표로 신체적 정신적 건강 상태를 유지하게 하는 비제약적 전기처방(ElectRx, electrical prescription) 프로그램을 운영하고 있다. 이 프로그램에서는 폐-루프 최소침습 또는 비침습적인 방법으로 말초신경을 자극하여 통증, 종합감염, 불안장애, 그리고 외상 후 스트레스 장애를 극복하는 기술을 개발하고 있다[43].
국내의 경우 신경조절기술 관련 연구개발 사업은 진행되었지만 아직까지 전자약 관련된 연구개발사업은 진행된 바 없다. 최근 보건복지부와 한국보건산업진흥원은 산-학-연이 참가하여 ‘전자약 연구개발 사업’ 기획이 진행되고 있는데, 산업체의 경우 경두개 자극치료기 등을 개발하고 있는 벤처기업 중심으로 전자약 개발에 관심을 가지고 있다.
Ⅴ. 시장규모
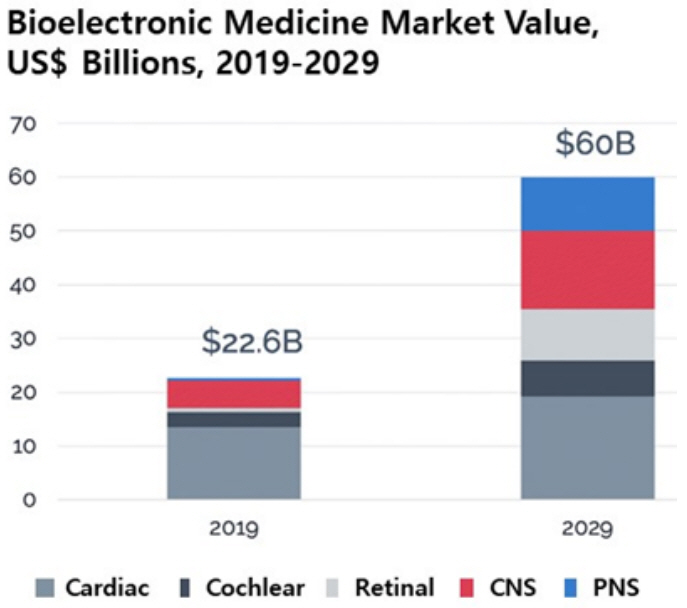
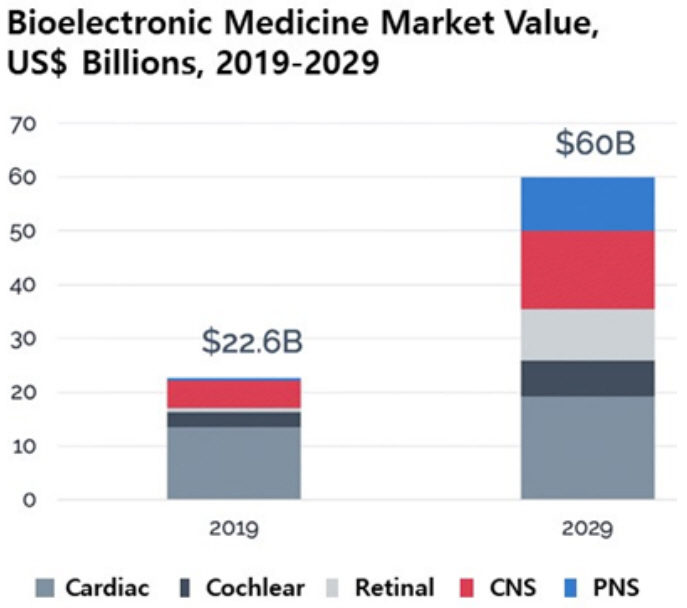
의료 시장에서는 전자약을 만성 질환의 치료 또는 완화를 위하여 전기자극을 사용하는 삽입형 및 비삽입형 의료 기기로 정의하고 있으며, 심박동기(Pacemakers), 척수자극기(SCS), DBS 등 기존의 신경조절기와 말초신경 자극기 등을 폭넓게 포함하고 있다. 이와 같은 전자약 시장은 최근 의료기기 가운데 가장 뜨거운 관심을 받고 있으며, 세계 유수의 시장조사 기관에서 시장 조사 결과를 발표하고 있다. Report & Data는 전 세계 전자약 시장을 2018년 200억 달러로 평가되었고, 2026년까지 8.5%의 성장률을 보이며 380억 달러에 이를 것으로 전망하고 있다[44]. Market & Market에 따르면 2016년 172억 달러(약 19조 7,000억 원) 규모의 세계 전자약 시장이 연간 7.9% 정도씩 성장하여 2021년에는 252억 달러(약 28조 9,000억 원)에 이를 것으로 전망하였으며, 치료제가 없는 질병에 대한 전자약 개발이 이루어진다면 관련 시장은 이보다 훨씬 커질 수 있을 것으로 예측하였다[45]. Verified Market Research는 세계 전자약 시장 규모가 20년에 240억 달러 그리고 2019~2026년 사이에 연간 8.9% 성장을 이뤄 2026년에는 470억 달러를 기록할 것으로 예측하였다[46]. 또한, IDTechEx는 전자약 시장이 매년 10% 이상의 성장하고, 2029년에는 600억 달러에 이를 것으로 전망하였다(그림 8)[47]. IDTechEx는 인공망막과 말초신경 자극 시장이 뇌신경 자극, 심박동 그리고 인공와우 시장에 비해 빠르게 성장할 것으로 예측하였다.
Ⅵ. 향후 전망
1990년대부터 뇌신경 자극을 기반으로 하는 뇌신경조절 기술이 뇌신경질환에 지속적으로 적용되어 왔으며, 근래에는 뇌신경에 비해 거부감이 상대적으로 적은 말초신경을 자극하여 뇌신경질환뿐만 아니라 부작용이 큰 기존의 약물을 대신하려는 시도가 진행되고 있다. 그동안 뇌신경 인터페이스와 신경보철을 위해 개발된 생체 적합성 소재, 고 신뢰성 고성능 신경전극, 소형화된 신경신호 처리 시스템, 인공지능 기능 소프트웨어 등은 말초신경 인터페이스를 근간으로 하는 전자약 기술의 기반이 되고 있다.
2018년 세계경제포럼에서 주목되는 10대 기술에 선정[48]된 전자약은 완치가 어려운 류마티스 관절염, 당뇨병, 배뇨장애, 천식, 소화불량과 같은 만성질환뿐만 아니라 통증, 심장병, 패혈성 쇼크, 치매, 파킨슨병, 우울증과 같은 난치병 치료 그리고 인지기능 향상에도 활용될 수 있기 때문에 관련 연구개발이 활발하게 진행 중이다. 말초신경과 장기와의 연결을 고려할 때 전자약은 질병 이외에도 체온유지, 에너지 항상성, 면역력 향상, 더 나아가 수명연장에도 기여할 가능성이 높다.
현재 미주신경자극 기반 간질 및 우울증 치료를 위한 전자약이 FDA 승인으로 시술되고 있지만, 그 작용 메커니즘은 여전히 미스터리로 남아 있다. 그리고 어느 환자에게는 유효하지만 다른 환자들에겐 유효하지 않는 문제점이 존재한다. 향후 새롭게 개발되는 전자약은 기존 신경조절용 전극에 비해 신경선택도가 높아져서 메커니즘 이해를 용이하게 하며, 개인 맞춤형으로 발전될 것으로 예상된다. 또한 당뇨병 적용 예시에서 기술한 바와 같이 폐루프 전자약 치료가 보편화될 것이다. 추가로 예를들면, 위장의 움직임을 감지하여 움직임의 가속과 억제를 조절하거나 방광압력을 측정하여 배뇨 상태를 조절하는 것이 이루어질 것이다. 궁극적으로 전자약이 보급되더라도 기존의 약물은 최소한으로 복용되어 전자약과 협업할 것으로 예상된다.
대사시스템과 신경계의 상호작용에 대한 이해 그리고 신경자극에 대한 대사시스템의 반응에 대한 충분한 검증은 전자약의 발전을 가속할 것으로 보인다. 상호작용에 대한 이해가 충분하지 못하여 자극-반응에 관한 수학적인 모델을 수립할 수 없는 현재 상태에서는 인공지능이 그 대안이 될 수 있다. 전자약 기술의 진보는 뇌신경조절과 마찬가지로 재료, 전기, 기계, 그리고 뇌 공학과 뇌 과학 등 다양한 분야의 긴밀한 협력에 의해 이루어지기 때문에 융합형 연구개발 프로그램이 요구된다. 또한, 전자약의 활성화와 보급은 이와 같은 다학제적 협력 이외에 법규 제정, 임상지원, 의료보험, 산업인프라 등 전자약 관련 생태계 구축을 필요로 한다.
2019년 상반기 FDA 및 CE 승인 건[49]이 모두 비삽입형임을 고려할 때 국내의 경우 관련 경험과 기술력 부족으로 산업체에서 삽입형 전자약에 대한 연구개발이 시도될 가능성은 낮으며, 따라서 단기적으로는 비삽입형 전자약 개발이 선행될 가능성이 높다. 현재 가장 단순한 구조를 가지면서 선택도가 가장 낮은 삽입형 cuff 전극의 경우에도 신뢰성이 충분하지 않은 문제가 있기 때문에 이의 해결이 시급하다. 말초신경전극의 신뢰성 문제는 뇌신경전극과 마찬가지로 가장 큰 난제로 여겨진다. 기술적 난이도가 높지만 의료적으로 가장 파급효과가 큰 삽입형 전자약의 경우 정부출연연구소와 학계에서 연구개발이 주도될 가능성이 높은데, 의료용 원천소재의 확보와 공정기술의 혁신 그리고 전 임상 및 임상평가 협력구축은 삽입형 전자약의 성능향상과 보급을 앞당길 것이다.
약어 정리
CE
Conformite European
DBS
Deep Brain Stimulation
DARPA
Defense Advanced Research Projects Agency
FDA
Food and Drug Administration
FINE
Flat Interface Neural Electrode
GSK
GlaxoSimthKline
LIFE
Longitudinal IntraFascicular Electrode
MEA
Multi-Electrode Array
NIH
National Institutes of Health
SCS
Spinal Cord Stimulation
SPARC
Stimulating Peripheral Activity to Relieve Conditions
TIME
Transverse Intrafascicular Multichannel Electrode
VNS
Vagus Nerve Stimulation
C. Bouton, "Bioelectronic medicine: molecular mechanisms," SRC/NSF Workshop on Microsyst for Bioelecton Med, IBM Conference Center, Washington, D.C., USA, Apr. 12–13, 2017.
S. Mishra, "Electroceuticals in medicine–The brave new future," Indian Heart J., vol. 69, no. 5, 2017, pp. 685-686.
B. J. Seicol et al., "Neuromodulation of metabolic functions: from pharmaceuticals to bioelectronics to biocircuits," J. Biol. Eng., vol. 13, 2019, Article no. 67.
K. Devarakonda and S. Stanley, "Investigating metabolic regulation using targeted neuromodulation," Ann. New Yorl Academy Sci., vol. 1411, no. 1, 2018, pp. 83–95.
R. Carnagarin et al., "Autonomic regulation of glucose homeostasis: a specific role for sympathetic nervous system activation," Curr. Diab. Rep., vol. 18, no. 11, 2018, doi:10.1007/s11892-018-1069-2.
P. S. Olofsson and K. J. Tracey, "Bioelectronic medicine: technology targeting molecular mechanisms for therapy," J. Intern. Med., vol. 282, no. 1, 2017, doi: 10.1111/joim.12624.
G. de Lartigue, "Role of the vagus nerve in the development and treatment of diet-induced obesity," J. Physiol., vol. 594, no. 20, 2016, doi: 10.1113/JP271538.
H. Divanovic et al., "Effects of electrical stimulation as a new method of treating diabetes on animal models: review," IFMBE Proc., vol. 62, 2017, doi: 10.1007/978-981-10-4166-2_38.
B. Thorens, "Neural regulation of pancreatic islet cell mass and function," Diabetes Obes. Metab., vol. 16, 2014, pp. 87–95.
U. S. Food and Drug Administration, "VNS therapy system: FDA," premarket approval (PMA)-Depression (Online) (updated 2005).
J. P. O’Reardon, P. Cristancho and A.D. Peshek, "Vagus nerve stimulation (VNS) and treatment of depression: to the brainstem and beyond," Psychiatry (Edgmont), vol. 3, no. 5, 2006, pp. 54–63.
L. K. McCorry, "Physiology of the autonomic nervous system," Am. J. Pharm. Educ., vol. 71, no. 4, 2007, Article no. 78, doi:10.5688/aj710478.
F. S. Routledge et al., "Improvements in heart rate variability with exercise therapy," Can. J. Cardiol., vol. 26, 2010, pp. 303–312.
A. Nesvold et al., "Increased heart rate vatiability during nondirective meditation," Eur. J. Prev. Cardiol., vol. 19, 2012, pp. 773–780.
S. Breit et al., "Vagus nerve as modulator of the brain-gut axis in psychiatric and inflammatory disorders," Front Psychiatry, vol. 9, 2018, Article no. 44, doi:10.3389/fpsyt.2018.00044.
B. Bonaz et al., "Vagus nerve stimulation: from epilepsy to the cholinergic anti-inflamatory pathway," Neurogastroenterol Motil, vol. 25, no. 3, 2013, pp. 208–221.
S. C. Payne, J. B. Furness and M. J. Stebbing, "Bioelectric neuromodulation for gastrointestinal disorders: effectiveness and mechanisms," Nat. Rev. Gastro. Hepat., vol. 16, no. 2, 2019, pp. 89–105.
U. S. Food and Drug Administration, "VNS therapy system: FDA, premarket approval (PMA)-Epilepsy" (Online) (updated 1997).
J. M. Morton et al., "Effect of vagal nerve blockade on moderate obesity with an obesity-related comorbid condition: the ReCharge Study," Obes. Surg., vol. 26, 2016, pp. 983–989.
U. S. Food and Drug Administration, "Devices@FDA: Medtronic interstim sacral nerve stimulation therapy system" (Online) (updated 2011).
L. V. Borovikova et al., "Vagus nerve stimulation attenuates the systemic inflammatory response to endotoxin," Nature, vol. 405, 2000, pp. 458–461.
F. A. Koopman et al., "Vagus nerve stimulation inhibits cytokine production and attenuates disease severity in rheumatoid arthritis," Proc. Natl. Acad. Sci. USA, vol. 113, no. 29, 2016, pp. 8284–8289.
S. Trevitt, S. Simpson, and A. Wood, "Artificial pancreas device systems for the closed-loop control of type 1 diabetes: What systems are in development?" J. Diabetes Sci. Technol., vol. 10, no. 3, 2016, pp. 714–723.
A. Haidar et al., "Comparison of dual-hormone artificial pancreas, single-hormone artificial pancreas, and conventional insulin pump therapy for glycaemic control in patients with type 1 diabetes: an open-label randomised controlled cross over trial," Lancet Diabetes Endocrinol., vol. 3, 2015, pp. 17–26.
A. Guemes and P. Georgiou, "Review of the role of the nervous system in glucose homeostasis and future perspectives towards the management of diabetes," Bioelectron Med., vol. 4, 2018, doi: 10.1186/s42234-018-0009-4.
C. M. Hales, "Prevalence of obesity among adults and youth: United States 2015–2016," NCHS Data Brief, vol. 288, 2017, pp. 1–8.
E. A, Katsareli and G. V. Dedoussis, "Biomarkers in the Field of obesity and its related comorbidities," Expert Opin. Ther. Targets, vol. 18, 2014. pp. 385–401.
R. Kassir et al., "Effects of vagus nerve stimulation on weight loss and associated disorders: a therapeutic perspective," J. Med. Diagn Meth., vol. 3, 2014, doi: 10.4172/2168-9784.1000e110.
M. L. Ganz et al., "Economic costs of over active bladder in the United States," Urology, vol. 75, 2010, pp. 526–532.
J. W. Boggs et al. "Frequency dependent selection of reflexes by pudendal afferents in the cat," J. Physiol., vol. 577, 2006, pp. 115–126.
X. Navarro et al., "A critical review of interfaces with the peripheral nervous system for the control of neuroprostheses and hybrid bionic systems," J. Peripher Nerv. Syst., vol. 10, 2005, pp. 229–258.
E. H. Rijnbeek, N. Eleveld, and W. Olthuis, "Update on peripheral nerve electrodes for closed-loop neuroprosthetics," Front Neurosci, vol. 12, 2018, doi:10.3389/fnins.2018.00350.
C. Russell, D. Roche, and S. Chakrabarty, "Peripheral nerve bionic interface: a review of electrodes," Int. J. Intell. Robot. Appl., vol. 3, 2019, pp. 11–18.
S. Eldabe, E. Buchser, and R.V. Duarte, "Complications of spinal cord stimulation and peripheral nerve stimulation techniques: a review of the literature," Pain Med, vol. 17, 2016, pp. 325–336.
V. H. Desai et al., "Chronic sensory-motor activity in behaving animals using regenerative multi-electrode interfaces," in Proc. Annu. Int. Conf. IEEE Eng. Med. Biol. Soc., Chicago, IL, USA, Aug. 2014, pp. 1973–1976.
X. A. Maul et al., "Microcurrent technology for rapid relief of sinus pain: a randomized placebo-controlled, double-blinded clinical trial," Int. Forum Allergy Rhinol., vol. 9, 2019, pp. 352–356.
K. Birmingham et al., "Bioelectronic medicines: a research roadmap," Nat. Rev. Drug Discov., vol. 13, 2014, pp. 399–400.
S. F. Cogan et al., "Tissue damage thresholds during therapeutic electrical stimulation," J. Neural Eng., vol. 13, 2016, doi: 10.1088/1741-2560/13/2/021001.
Markets & Markets, "Electroceuticals / bioelectric medicine market by product (pacemakers, cochlear implants, spinal cord stimulators), type of device (implantable, non-invasive), application (arrhythmia, depression, migraine), end user (hospitals) - Global Forecast to 2021."
Verified Market Research, "Global electroceuticals/bioelectric medicine market size by type, by product, by application, by geographic scope and forecast," 2019.
Alliance for Advancing Bioelectronic Medicine, "Building a bioelectronic medicine movement 2019: insights from leaders in industry, academia, and research," Bioelectron Med, vol. 6, 2020, 1.
그림 1
(a) 신경자극에 의해 대사조절이 가능한 장기 (b) 약물치료에 의한 대사조절 (c) 전기자극에 의한 질환치료 (d) 줄기세포 등 인공조직 대체
출처 Reprinted from B. J. Seicol et al., “Neuromodulation of metabolic functions: from pharmaceuticals to bioelectronics to biocircuits,” J. Biol. Eng., Vol. 13, 2019, 67:1-12. CC BY 4.0.
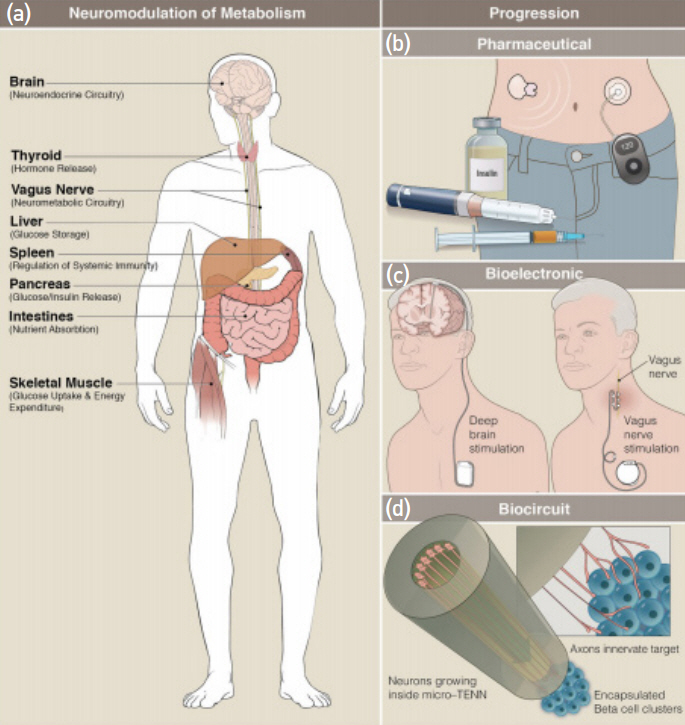
그림 2
(a) 휴먼 신경계와 (b) 말초신경-장기 연결도
출처 (a) 게티이미지뱅크, 무단 전재 및 재배포 금지, (b) BruceBlaus, "Medical gallery of Blausen Medical 2014," WikiJournal of Medicine 1 (2). DOI:10.15347/wjm/2014.010 CC BY 3.0.
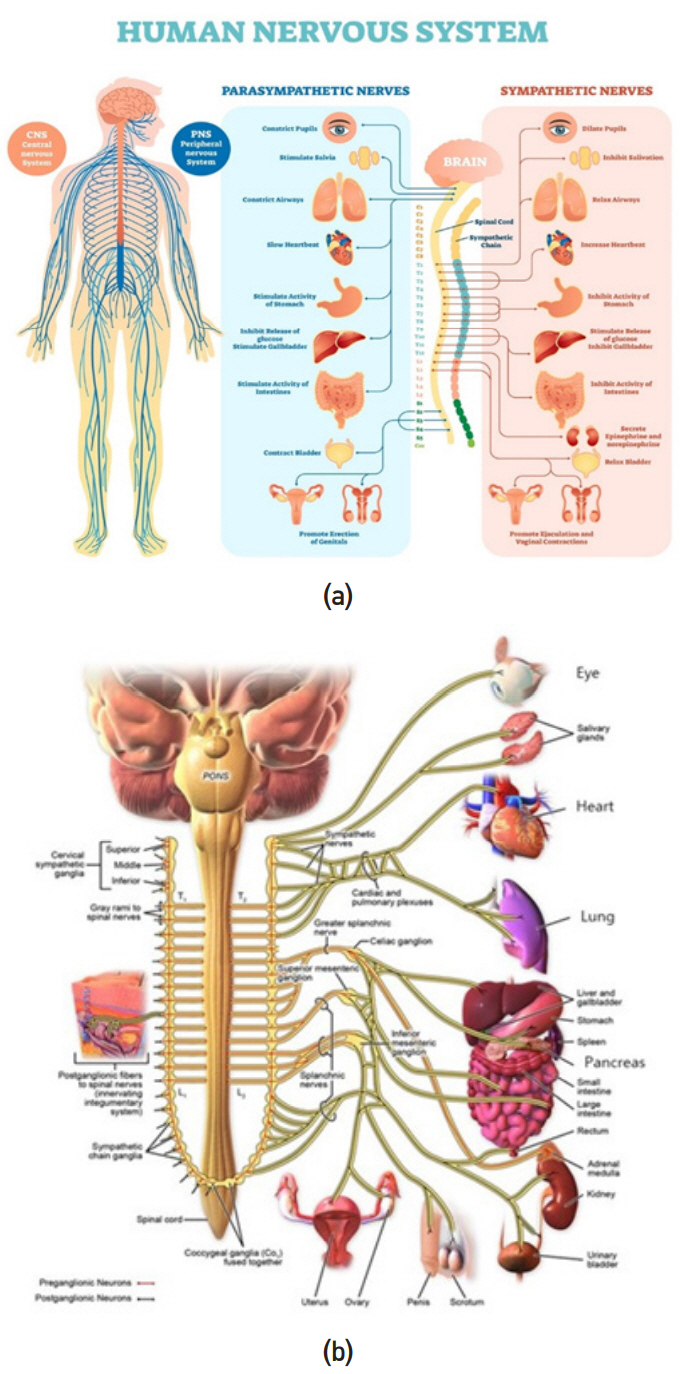
그림 3
미주신경 자극을 통한 류마티스 관절염 치료 메커니즘
출처 F.A. Koopman et al., “Vagus nerve stimulation: A new bioelectronics approach to treat rheumatoid arthritis?” Best Practice Res. Clinical Rheumatology, vol. 28, no. 4, 2014, pp. 625-635, CC BY-NC-ND 3.0.

그림 4
미주신경 자극에 의한 혈당조절 메커니즘
출처 https://bigthink.com/philip-perry/darpa-is-investing-in-a-platform-that-accelerates-learning
- Sign Up
- 전자통신동향분석 이메일 전자저널 구독을 원하시는 경우 정확한 이메일 주소를 입력하시기 바랍니다.