수계전해질기반 차세대 금속이온전지 기술
Technologies for Next-Generation Metal-Ion Batteries Based on Aqueous Electrolytes
- 저자
-
신동옥스마트소재연구실 doshin@etri.re.kr 최재철스마트소재연구실 jaecheol.choi@etri.re.kr 강석훈스마트소재연구실 shkang@etri.re.kr 박영삼스마트소재연구실 s_yspark@etri.re.kr 이영기스마트소재연구실 lyg@etri.re.kr
- 권호
- 39권 1호 (통권 206)
- 논문구분
- 일반논문
- 페이지
- 83-94
- 발행일자
- 2024.02.01
- DOI
- 10.22648/ETRI.2024.J.390108
 본 저작물은 공공누리 제4유형: 출처표시 + 상업적이용금지 + 변경금지 조건에 따라 이용할 수 있습니다.
본 저작물은 공공누리 제4유형: 출처표시 + 상업적이용금지 + 변경금지 조건에 따라 이용할 수 있습니다.- 초록
- There have been continuous requirements for developing more reliable energy storage systems that could address unsolved problems in conventional lithium-ion batteries (LIBs) and thus be a proper option for large-scale applications like energy storage system (ESS). As a promising solution, aqueous metal-ion batteries (AMIBs) where water is used as a primary electrolyte solvent, have been emerging owing to excellent safety, cost-effectiveness, and eco-friendly feature. Particularly, AMIBs adopting mutivalence metal ions (Ca2+, Mg2+, Zn2+, and Al3+) as mobile charge carriers has been paid much attention because of their abundance on globe and high volumetric capacity. In this research trend review, one of the most popular AMIBs, zinc-ion batteries (ZIBs), will be discussed. Since it is well-known that ZIBs suffer from various (electro) chemical/physical side reactions, we introduce the challenges and recent advances in the study of ZIBs mainly focusing on widening the electrochemical window of aqueous electrolytes as well as improving electrochemical properties of cathode, and anode materials.
Share
Ⅰ. 서론
온실가스 배출과 이로 인한 글로벌 기후변화 문제를 극복하기 위해 기존의 화석연료에 대한 의존을 낮추고 지속 가능한 청정 에너지원을 확보하기 위한 방법으로 에너지 저장 소자 개발이 전 세계적으로 이루어지고 있다. 지속적인 충방전을 통해 에너지 저장 소자로 활용되는 이차전지는 그 응용 범위가 기존 핸드폰 및 노트북 등의 소형 전원에서 현재는 전기자동차(EV: Electric Vehicle)와 에너지저장시스템(ESS: Energy Storage System) 등의 중대형 전원으로 그 응용처의 규모가 커지고 있으며, 관련 시장에서도 중대형 이차전지의 비중이 증가하고 있는 추세이다. 특히, 신재생 에너지와 분산형 발전 비율이 높아지고 있으며 이를 대응하기 위해 대규모 에너지저장시스템에 대한 이차전지 수요가 급격히 증가하고 있다. 대표적인 이차전지로, 높은 구동 전압 및 에너지 밀도, 고출력 및 장수명 특성으로 인해 리튬이온전지(LIBs: Lithium-Ion Batteries)가 선택되어 그 수요를 충당하고 있다.
그러나 기존 상용화된 리튬이온전지는 가연성 유기계 액체전해질을 기반으로 구동하여 잠재적으로 발화, 누액 및 폭발 등 심각한 안전성 문제를 내포하고 있는데, ESS와 같이 대규모 시설의 경우 용량 규모에 비례하여 피해 규모도 커지게 된다. 또한, 제조 공정 간 탄소 배출이 높고 유해 물질의 배출이 불가피하며 제조 단계 및 사용 후 폐기물 처리 비용이 높다는 문제점이 있다. 뿐만 아니라 시장 규모가 급속히 성장하고 있는 중대형 이차전지 부분 수요를 리튬이온전지로 대응한다는 것은 매장량이 제한된 자원에 의존, 불균형적인 글로벌 자원 분포 환경 및 자국 경제 보호를 우선시하는 국제 정세를 고려했을 때, 자원 수급 불안정성과 이로 인한 가격 변동의 영향으로 안정적인 산업 환경 형성에 많은 제한을 받게 된다. 이에 기존 리튬이온전지의 문제점을 해결하기 위한 시스템으로 전고체 이차전지가 개발되고 많은 각광을 받고 있다. 액체전해질을 고체전해질로 대체하여 안전성을 획기적으로 개선시킬 수 있지만, 상대적으로 낮은 이온전도도, 고체전해질/전극 계면 및 전극 내 고체전해질/활물질 계면에서 높은 저항 및 부반응 발생 등 소재 특성 및 공정상 해결해야 할 이슈가 있으며, 여전히 리튬자원 의존성이 높고 제조 공정 간 높은 비용, 대면적화의 어려움 및 환경 유해성 소재 적용 등으로 인해 군용 무인 차량이나 우주 탐사 차량 등 특수목적용으로 상용화가 우선적으로 예상된다.
기존 리튬이온전지 및 전고체 이차전지를 대체하여 상기 언급된 문제점들을 해결하기 위해 수계형 금속이온전지(AMIBs: Aqueous Metal Ion Batteries) 시스템을 개발하려는 시도가 활발히 진행되고 있다. 수계형 금속이온전지는 물을 기반으로 하는 수계전해질을 사용하여 친환경성, 저비용, 높은 안전성 및 높은 이온전도도 등의 장점들을 보여주며 Li+, Na+, K+ 등의 1가 금속이온 또는 Zn2+, Ca2+, Mg2+, Al3+ 등의 다가 금속이온을 기반으로 하고 있다. 특히, 다가 금속이온의 경우 이온당 전달할 수 있는 전자가 2개 이상으로 이론적으로 부피당 에너지 밀도가 매우 높고 리튬자원대비 매장량이 풍부하며 원료 소재의 가격이 낮다는 장점이 있다. 따라서, 수계형 다가 금속이온전지는 작은 공간에 배치되어 높은 무게당/부피당 에너지 밀도가 요구되는 소형 모바일 기기나 전기자동차보다는 안전성과 저비용을 우선시하고 무게와 부피에 구애받지 않는 ESS용으로 최적 이차전지 시스템이 될 수 있다. 이중, 수계형 아연이온전지(AZIBs: Aqueous Zinc Ion Batteries)가 상대적으로 높은 안정성, 높은 용량 및 낮은 비용으로 인해 다른 다가 금속이온전지 대비 많은 주목을 받고 연구가 진행되고 있다(그림 1) [1,2]. 아연(~US$2.4/kg)은 다른 알칼리 금속들(Li: ~US$19.2/kg, Na: ~US$3.1/kg, K: ~US$13.1/kg) 대비 저렴하고 아연이온전지의 일반적인 양극 소재인 MnO2(~US$1.7/kg)와 V2O5(~US$5.5/kg)가 기존 리튬이온전지 양극 소재인 LiCoO2(~US$55/kg), Li(NiMNCo)O2(~US$34/kg)보다 가격이 상당히 낮다[3]. 또한, 아연이온전지에 사용되는 수계형 전해질은 매우 안전하고 높은 이온전도도(0.1~5S/cm)를 나타낸다. 그림 2(a)는 기존 리튬이온전지와 아연이온전지 특성 비교를 나타내고 있다. 구동 메커니즘을 보여주는 스킴(그림 2(b))을 통해 충방전이 가능한 아연이온전지는 Zn 염이 해리된 전해질, 아연이온(Zn2+)이 저장될 수 있는 양극 및 Zn금속 음극으로 구성되고, 충방전 간 Zn2+가 전해질을 통해 양/음극 사이를 이동하면서 양극에서 삽입/탈리, 음극에서는 전착/탈착 거동을 통해 전체적인 시스템이 구동되고 있음을 알 수 있다[3].
그림 1
다양한 에너지 저장 장치 시스템의 중량당 출력 밀도 대 에너지 밀도 비교
출처 Reprinted with permission from [1], ⓒ 2022, American Chemical Society.
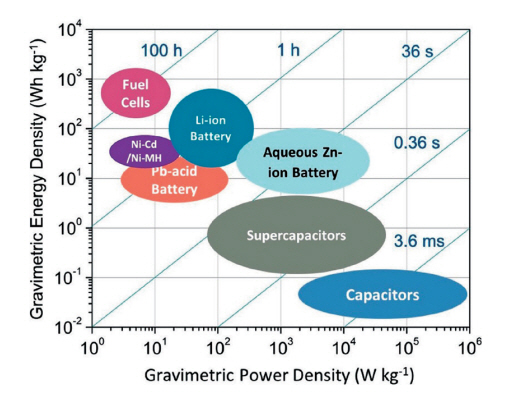
그림 2
(a) 기존 리튬이온전지와 수계형 아연이온전지 특성 비교, (b) 아연이온전지 구성 및 구동 메커니즘
출처 Reprinted with permission from [3], ⓒ 2020, Royal Society of Chemistry

상기 언급된 수계형 아연이온전지의 장점에도 불구하고 상업적으로 적용 가능한 이차전지 시스템으로 발전시키기 위해서는 극복해야 할 문제점들이 있다. 먼저, 용매인 물의 좁은 안정 전위창(1.23V)으로 인해 전해질 분해 및 수소 발생이 쉽게 발생하여 고전압 구동이 어렵다[4]. 기존 양극 소재의 경우 대부분 낮은 전압에서 구동되는 소재들에 대한 연구들이 보고되었으며, 용출 및 산소발생 현상 등에 의해 가역성이 감소되고 저항이 증가하고, Zn금속 음극의 경우 부식 현상 및 수지상(Dendrite) 성장 등의 부반응에 의해 Zn금속 전탈착 효율이 현저히 낮아진다[5].
본고에서는 수계형 다가 금속이온전지의 대표적인 모델 시스템인 아연이온전지의 주요 구성 요소인 수계전해질, 양극, 음극에 대해 주제별로 나눠 연구 동향을 소개하고자 한다. 특히, 기존 아연이온전지의 전기화학적 성능을 개선시키기 위해 수행된 연구들에 대해 소재적인 관점에서 다루고 나아가 전반적인 수계형 이차전지 시스템의 발전 방향에 대해 논의하고자 한다.
Ⅱ. 수계전해질
일반적으로 Zn염이 포함된 중성 또는 약산성의 전해질이 상대적으로 장시간 충방전이 가능하고 안정한 특성을 보여 아연이온전지용 전해질로 활용되고 있다. 대표적인 Zn염으로는 ZnSO4, Zn(CF3SO3)2, ZnCl2, ZnF2, Zn(NO3)2, Zn(ClO4)2, Zn(CH3COO)2, Zn(BF4)2, Zn(PF6)2, Zn(TFSI) 등이 사용되고 있으며, 용매로는 물이 사용되고 있는 한편, 비수계전해질 용매로는 유기용매, 이온성 액체, DES 등이 사용되고 있다. 수계전해질은 자체 Zn2+ 수송률이 매우 높고 전극/전해질 계면에서의 계면 저항(Interfacial resistance, Rif)이 비수계 전해질에 비해 낮아 고출력 충방전이 가능하다. 그러나 물 분해반응이 상대적으로 낮은 전압에서도 쉽게 발생하여 고전압 양극 소재 적용이 어려워 비수계전해질 기반 이차전지에 비해 에너지 밀도가 현저히 낮다. 또한, 중성 또는 약산성 분위기에서 Zn음극과 집전체의 부식 등 열화현상이 발생하여 수명 특성이 저하되기 쉽다. 수계전해질의 고전압 및 화학적 안정성, 이온전도도, 쿨롱 효율 등 전기화학적 특성 및 성능을 개선시키기 위해 많은 기초연구가 진행되고 있으며, 전해질을 구성하는 요소별로 최근 진행된 연구 동향에 대해 소개하고자 한다.
1. 전해질 염
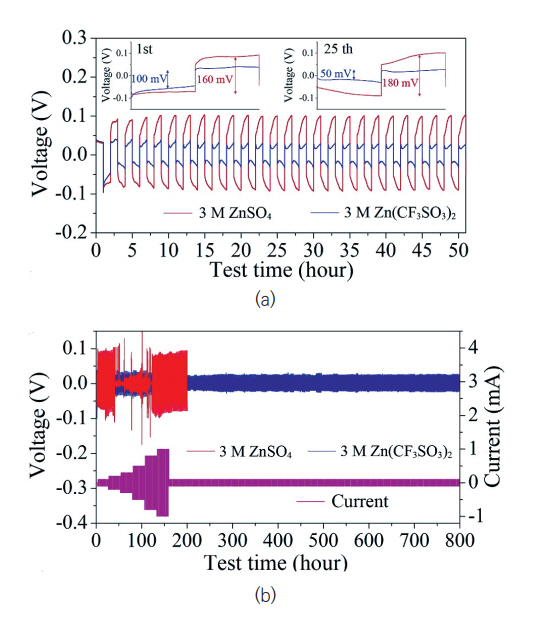
전해질 염은 전해질 용매에 해리되어 실질적으로 양극과 음극 사이를 이동하는 금속이온을 제공하는 역할을 한다. 여러 가지 Zn염 중에서 부식성이 강한 ZnCl2, Zn(NO3)2에 비해 ZnSO4, Zn(CF3SO3)2 (또는 Zn(OTf)2)이 Zn금속 음극을 보다 안정화시킬 수 있다고 알려져 있다. Zn(CF3SO3)2염의 경우 농도가 증가함에 따라 이온전도도는 감소하고 점도는 증가하는데 3몰 농도의 Zn(CF3SO3)2 염을 포함하는 수계전해질은 ~2.5V에 이르는 전기화학적 전위창, 3.47S/cm의 이온전도도 및 Zn 전착/탈착 시 낮은 과전압과 100%에 이르는 쿨롱 효율을 보이는 반면, 3몰 농도의 ZnSO4 염의 경우 높은 과전압과 좋지 못한 수명 특성을 보였다(그림 3) [6]. 이처럼 Zn(CF3SO3)2 염의 우수한 전기화학적 특성은 상대적으로 SO42-보다 부피가 큰(Bulky) CF3SO3- 음이온으로 인하여 Zn2+을 둘러싸고 있는 물 분자의 수를 줄여 용매화 효과를 감소시키기 때문이다.
그림 3
(a) Zn염에 따른 Zn/Zn 대칭셀 결과, (b) Zn염에 따른 Zn/Zn 대칭셀의 율속 및 장수명 결과
출처 Reproduced with permission from [6], ⓒ 2016, American Chemical Society.
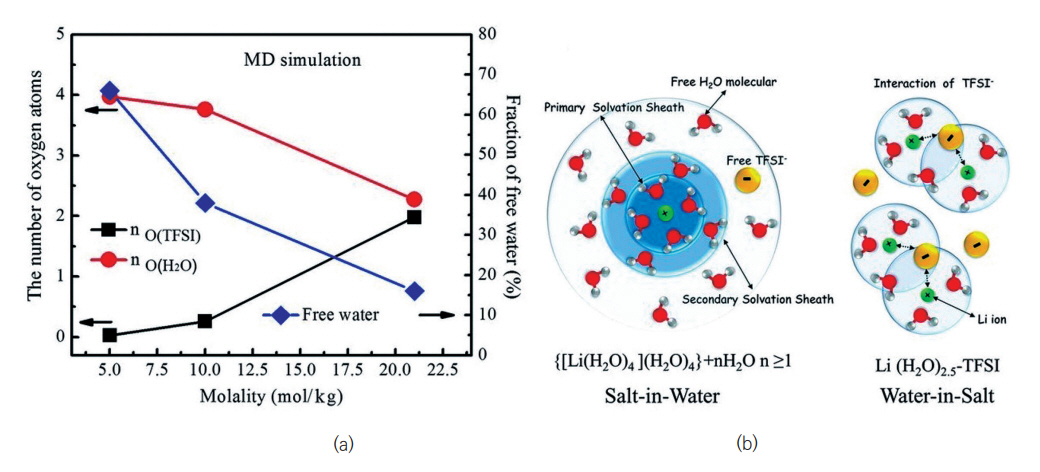
한편, 전해질 염의 농도는 전체적인 전해질의 전기화학 성능에 영향을 줄 수 있는 인자이다. 높은 염농도는 물의 활성도를 낮춰 분해반응을 억제함으로 써 구동 시 전해질의 안정성을 높일 수 있어 쿨롱 효율 및 수명 특성을 향상시킬 수 있다. 따라서, 전해질 염의 고농도화 전략은 기존 전해질의 좁은 구동 전압 범위(<2V)에 따른 저전압 구동 전극 적용 한계를 해결하여 궁극적으로 에너지밀도를 향상시킬 수 있는 방법으로 보고되고 있다. 수계전해질 염의 고농도화 방법은 21몰의 LiTFSI염이 포함된 전해질 연구를 통해 최초로 보고되었다[7]. 상대적으로 낮은 저농도 염 전해질에서는 Li 양이온이 우선용매껍질(PSS: Primary Solvation Sheath) 내에서 물 분자에 의해 둘러싸여 있고, 리튬화 전압이 물의 환원 전압보다 낮기 때문에 물의 환원이 우선적으로 발생한다. 반면, 고농도 염 전해질에서는 PSS에 평균적으로 Li 양이온당 2개의 TFSI- 음이온이 위치하게 되고 물보다 먼저 환원되는 반응을 통해 물의 환원을 최대한 억제하여 전해질의 작동 전압 범위를 확장할 수 있게 된다(그림 4). 같은 고농도 염 전략이 수계형 아연이온전지에서도 적용되었다. 1몰의 Zn(TFSI)2와 20몰의 LITFSI의 염이 함께 혼합된 고농도 염 전해질을 기반으로 한 Zn/Zn 대칭셀은 Zn의 전착/탈착 과정에서 수지상 형성이 없었으며 100%에 가까운 쿨롱 효율을 나타내었고, Zn/LiMn2O4 셀은 4,000 사이클 이상에서 80%의 용량유지율을 보이면서 180Wh/kg의 에너지 밀도를 보였다[8]. 비교 실험으로 1몰의 Zn(TFSI)2와 5몰의 LITFSI의 혼합염의 경우 Zn2+을 평균 6개의 물 분자에 의해 Zn2+가 둘러싸였으며, 1몰의 Zn(TFSI)2와 10몰의 LITFSI의 혼합염의 경우 TFSI- 음이온이 Zn2+의 PSS를 차지하기 시작하였다. 결국 최적화 조성인 1몰의 Zn(TFSI)2와 20몰의 LITFSI의 혼합염에서 Zn2+ 주위를 TFSI- 음이온이 차지하여 물의 환원을 억제하고 저전압대에서 수소 환원 발생이 방지된다. 고농도 염 방법은 전해질의 구동 전압 범위를 확장시킬 수 있는 효과적인 전략으로 염의 음이온에 의해 물의 용매화작용을 변화시킨다는 면에서 학문적으로 굉장히 참신하지만, 10몰 이상의 고농도화를 위해 고가의 염 소재 투입에 따른 전해질의 단가가 높아져 가격 경쟁력이 떨어지므로 실질적으로 산업 공정에 적용시키기 어렵다는 문제가 있다. 저가의 염 소재 개발 및 낮은 농도에서 유사한 거동을 구현하는 것이 보다 현실적이라고 볼 수 있다.
2. 겔 고분자 전해질
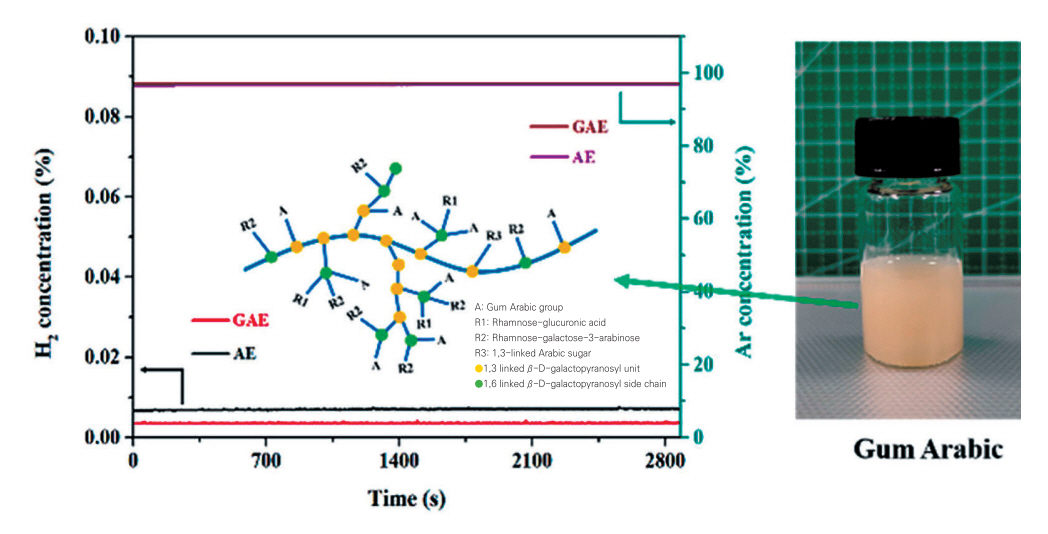
겔 고분자 전해질 또는 하이드로겔 전해질은 물리적 또는 화학적으로 가교된 친수성 고분자 프레임에 염이 녹아있는 물이 함침된 구조를 가지며 액체전해질과 유사한 높은 이온전도도와 고체와 같은 기계적 안정성이 있어 플렉서블 또는 웨어러블 아연이온전지에 활용될 수 있다. 일반적으로 poly(vinylidenefluoride-co-hexafluoropropylene)(PVDF-HFP), polyethylene oxide(PEO) 등이 겔 고분자 전해질에 연구되어 왔으나 낮은 이온전도도, 높은 계면 저항, 빠른 고분자 열화 및 낮은 기계적 강도로 인하여 아연이온전지 적용에 적합하지 않았다. 최근에는 수계형 고분자인 polyacrylic acid(PAA), poly(vinyl alcohol)(PVA), polyacrylamide(PAM), 젤라틴(Gelatin) 등이 하이드로겔 전해질로 활용되어 기존 액체전해질과 분리막 역할을 동시에 하면서 높은 화학적 안정성과 기계적 강도 특성을 보이고 있다. PEO와 Zn(CF3SO3)2 염으로 구성된 건식 고체 고분자 전해질(SPE: solid polymer electrolyte)이 핫 프레싱 공정으로 제조되었는데 PEO와 Zn(CF3SO3)2 염의 무게비가 90:10에서 상온에서 가장 높은 이온전도도(~1.09×10-6S/cm)를 나타내었다. 이는 염의 첨가로 인해 고분자 매트릭스 내 비정질 영역이 증가하기 때문이다[9]. 젤라틴은 프롤린, 하이드록시프롤린 및 글리신으로 이루어진 천연 고분자로 콜라겐으로부터 얻어지며, 높은 온도에서 물에 녹인 후 냉각과정을 통해 하이드로겔을 형성한다. 0.5몰 Li2SO4와 0.5몰 ZnSO4 염을 함유한 젤라틴 하이드로겔에 대한 연구가 수행되었는데 6.15×10-3S/cm의 이온전도도를 나타내었고, 냉각 온도가 25℃ 경우 대비 5℃인 경우 약 2배 높은 압축강도를 나타내었다[10]. 젤라틴 하이드로겔(GHE: Gelatin hydrogel electrolyte) 기반 Zn/Zn 대칭셀의 경우 일반적인 수계전해질 대비 Zn 수지상 형성 없이 낮은 과전압을 보여 800시간 이상의 안정적인 사이클 성능을 보였고, Zn/GHE/LMO(LiMn2O4)로 구성된 고체형 전지는 굽힘이나 비틀림 조건에서도 안정적으로 전자기기를 작동시킬 수 있었다. 한편, 젤라틴 하이드로겔에 가지형으로 PAM을 결합시킨 후 전기방사기반으로 제조된 PAN 멤브레인에 채워 제조된 계층적 구조의 고분자 전해질(HPE: Hierarchical Polymer Electrolyte)은 유연한 필름 형태로 3차원 형태의 매우 높은 기공구조를 보여 물 흡수율이 높아 빠른 이온 수송이 가능하다[11]. 그 결과, 상온에서 단순 젤라틴 전해질의 이온전도도(5.68×10-3S/cm)에 비해 1.76×10-2S/cm의 높은 이온전도도를 나타내면서 안정적인 기계적 특성도 보였다. 더욱이 α-MnO2와 카본나노튜브로 이루어진 양극과 Zn와 카본나노튜브로 이루어진 음극 사이에 HPE로 구성된 전지는 매우 높은 유연성과 안정성을 보였고, 6.18mWh/cm2, 148.2mW/cm2의 면적당 에너지밀도와 출력밀도를 나타내었으며, 1,000사이클 이후 97%의 용량유지율을 나타내었다. 최근에는 친환경적인 생분해성 고분자인 아라비아검을 이용한 겔 전해질 연구가 진행되었고, 이를 아연이온전지에 적용, 아라비아검과 물 사이 형성된 수소결합 네트워크로 인하여 물의 분해반응이 억제되었다(그림 5) [12]. 또한, Zn대칭셀 테스트 결과 Zn전극에서의 수소발생이 급감하여 수지상 형성 등 부반응 발생물 생성도 억제되었다.
그림 5
아라비아검기반 겔 전해질의 수소환원 발생 억제 특성 및 아라비아검 전해질 이미지
출처 Reprinted with permission from [12], ⓒ 2022, American Chemical Society.
3. 첨가제
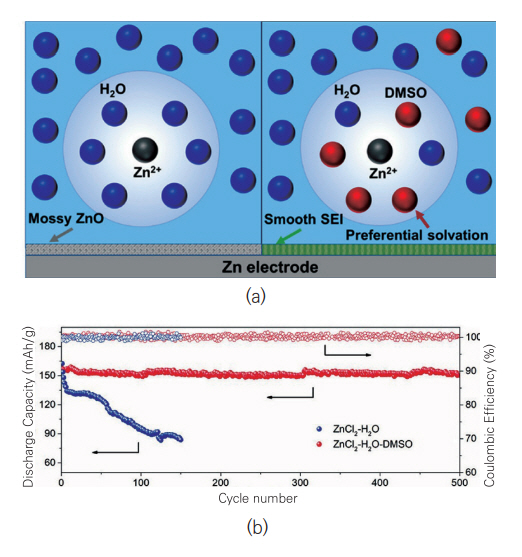
첨가제는 주로 유기물이나 금속이온으로 전해질에 소량 첨가되어 양극 용해 억제, 균일한 Zn의 전착/탈착 유도를 통한 수지상 형성 억제, 안정적인 SEI층의 형성 또는 전해질 내 용매화 구조를 변형시켜 구동 전압 범위를 확장시켜 에너지 밀도를 높이는 방법으로 사용되어왔다. 대표적인 예로 Na2SO4를 ZnSO4 전해질에 첨가하여 정전기적 쉴드 메커니즘을 활용한 연구가 수행되었다. Zn음극에 형성된 수지상 표면을 소듐 이온이 덮어 양전하의 반발 효과로 같은 양이온인 Zn2+의 전착을 막아 추가적인 수지상 형성을 억제하는 원리이다[13]. 첨가제를 통해 구동 전압을 확장시키기 위한 전략으로 Dimethyl Sulfoxide(DMSO)를 활용한 연구가 수행되었다[14]. ZnCl2/H2O로 구성된 전해질에 DMSO를 첨가하여 DMSO가 Zn2+의 우선용매껍질에 위치하여 물 분자와 강한 결합을 형성하여 물의 분해반응을 억제하는 원리이다(그림 6). 또한, Zn12(SO4)3Cl3(OH)15·5H2O, ZnSO3, ZnS가 풍부한 SEI층이 Zn음극 표면에 형성되어 Zn수지상 형성도 억제하였다. ZnCl2/H2O/DMSO로 이루어진 전해질 기반으로 제조된 Zn/Ti 반전지는 400사이클 이후에도 99.5%의 쿨롱 효율을 보였고, Zn/MnO2 완전지는 212Wh/kg의 에너지 밀도와 8C의 전류밀도로 500사이클 이후에도 95.3%의 용량유지율을 나타내었다.
그림 6
(a) H2O와 H2O/DMSO에서의 Zn2+의 용매화 구조 비교, (b) DMSO 첨가제 효과에 대한 Zn/MnO2 셀의 수명 특성 결과 비교
출처 Reproduced with permission from [14], ⓒ 2014, American Chemical Society
Ⅲ. 양극 소재
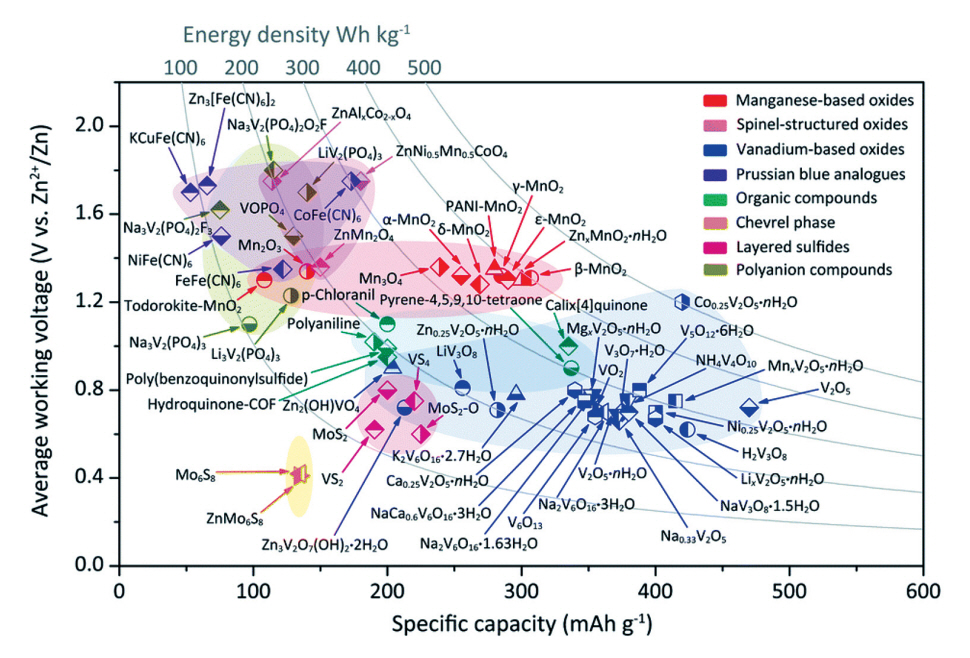
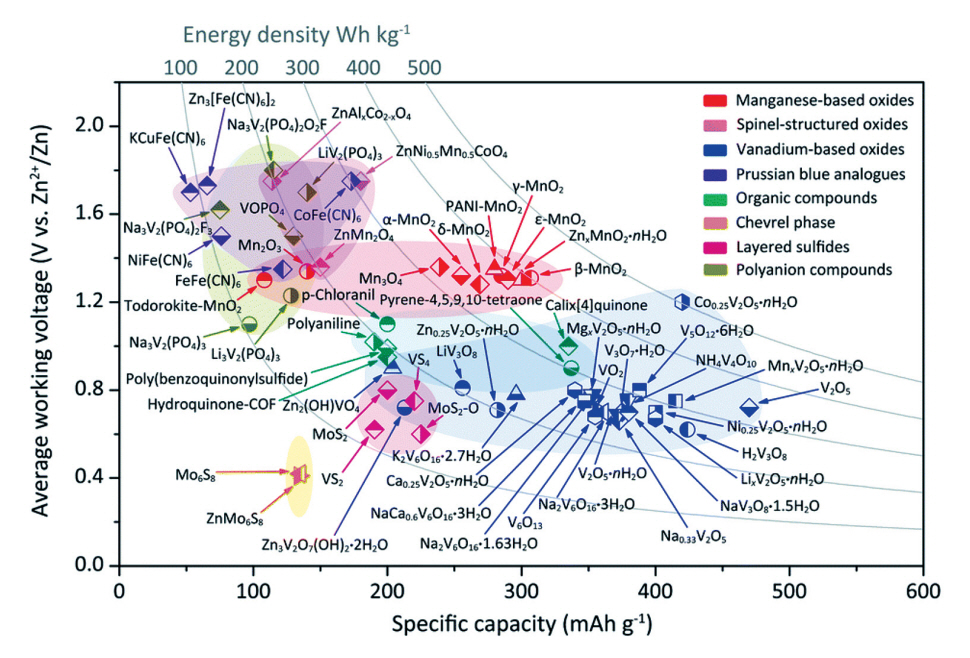
리튬이온전지에서와 같이 아연이온전지에서도 높은 구동전압, 가역적인 용량 및 수명 특성을 구현하는 양극 소재의 개발이 요구되고 있다. 수계용 금속이온전지용 양극 소재로는 망간 또는 바나듐기반 산화물, 프루시안 블루계 소재, 스피넬구조 산화물, 유기소재, 쉐브럴상 복합체 등이 있으며, 망간계 산화물과 바나듐계 산화물이 대표적으로 활용되고 있고 각기 다른 구조, 구현 용량, 평균 구동전압 및 반응 메커니즘을 보이고 있다(그림 7) [3]. 망간계 산화물은 매장량이 많아 저가이고 친환경적인 소재로써 많은 각광을 받아왔다. 최근에는 MnO2, Mn2O3, Mn3O4와 같은 소재들이 아연이온전지 양극으로 연구되어 왔으며, 이중 MnO2는 308mAh/g의 높은 비용량과 ~1.35V의 적절한 방전 전압을 보이고 있다. 수계전해질에서 MnO2는 소재의 구조 변형과 용해현상으로 인해 급격히 용량이 감소하는 열화현상을 보인다. 이를 억제하기 위해 사전에 Mn2+염을 전해질에 넣는 연구가 진행되었다. 0.1몰 MnSO4와 2몰 ZnSO4의 전해질 도입을 통해 α-MnO2 양극의 안정성이 개선되어 1.44V의 구동전압, 285mAh/g의 비용량 및 5,000사이클 이후에서 92%의 용량 유지율을 나타내었고, Zn금속 음극 또한 역시 안정화되었다[15]. MnO2의 또 다른 문제점으로는 낮은 전자전도도를 보인다는 것이다. 이를 개선시키기 위한 일반적인 방법으로 전도성 나노스케일의 탄소계 소재를 전극 내 포함시키는 연구들이 수행되어왔다. 한 예로 흑연판상에 MnO2를 형성시킨 소재는 매우 낮은 전하 이동 저항을 보여 빠른 Zn2+의 삽입/탈리 현상을 유도함으로써 높은 초기 방전 비용량(235mAh/g)을 나타내었다[16]. 망간계 산화물과 더불어 바나듐계 산화물이 다양한 바나듐의 산화수(V2+, V3+, V4+, V5+)에 따른 다수의 전자 레독스 반응, 높은 용량(>300mAh/g), 넓은 이온 전달 경로의 장점으로 인해 양극 소재로 많은 관심을 받고 있다. 다만, 평균 구동 전압이 0.8V로 에너지밀도가 제한된다. V2O5를 양극으로, 3몰 ZnSO4를 전해질로 활용하여 매우 우수한 Zn2+ 저장특성을 가지는 아연이온전지 연구결과가 보고되었다[17]. V2O5는 층상형 구조를 가지는데 각층은 반데르발스힘으로 접촉되어 있어 Zn2+저장에 충분한 공간이 제공될 수 있다. 그 결과 0.5A/g 전류밀도로 100사이클 이후에도 128mAh/g의 비용량을 나타내었다. 순환주사전압법 분석을 통해 V2O5에 삽입된 일부 Zn2+가 탈리되지 못하여 초기 가역용량이 감소되는 현상이 발생하였으나 구조 내 남은 Zn2+가 기둥역할을 하여 V2O5 구조의 안정화에 기여하여 안정적인 충방전 특성을 유도함이 밝혀졌다. 다른 바나듐계 산화물로 VO2는 수열합성, 용매열합성 등 상대적으로 낮은 온도에서 합성 가능하며, 구조 내 충분한 공간으로 인해 Zn2+의 삽입이 용이하다. 최근 환원된 그래핀옥사이드와 VO2의 복합제를 양극으로 활용한 아연이온전지에 대한 연구가 수행되었다. rGo/VO2 복합체는 3차원적인 기공 구조를 가지고 있어 높은 비표면적(251m2/g)을 보여 내부 이온전달이 유리하여 3몰 Zn(CF2SO3)2를 포함한 전해액을 이용하여 셀을 구동시킨 결과 35A/g의 초고속 전류밀도에서 120mAh/g의 방전 용량을 나타내었다[18].
그림 7
대표적인 아연이온전지의 양극 소재의 구동전압대 비용량 그래프
출처 Reproduced with permission from [3], ⓒ 2020, Royal Society of Chemistry.
Ⅳ. 음극 소재
아연이온전지 내 Zn금속 음극에서의 Zn2+의 저장은 가역적인 전착/탈착 메커니즘으로 설명된다. 충전 시 전착된 Zn2+는 방전 시 탈착되고 산화되어 전해질 내에서 용해된 이온으로 전환되어 전기장에 의해 양극 쪽으로 이동한다. 그러나 Zn2+의 전착/탈착은 음극 표면에서 균일하게 일어나지 않고 국부적으로 전류밀도가 높은 지역에 우선적으로 전착되어 수지상 형성이 유도된다. Zn수지상 형성은 표면적 증가, 용량 감소, 저항 증가 등으로 부식이나 수소발생반응 등의 부반응을 더욱 악화시키면서 추가적인 Zn수지상 형성을 유도하는 악순환 과정을 발생시킨다. 평탄한 Zn전극의 경우 전해질과 닿는 비표면적이 적어 불균일한 분포의 전류밀도와 이온농도가 발생하여 Zn수지상이 쉽게 형성된다. 이에 반해 3차원 구조의 Zn전극은 전극 구조의 변화에 붕괴에 대한 저항이 크고 넓은 이온전달경로가 확보되어 전극 내 이온수송률을 높이고 충분한 핵생성 자리를 제공하여 균일한 Zn2+의 전착을 유도할 수 있다. 따라서, 3차원 구조의 Zn전극은 수지상 형성 억제, 낮은 과전압을 통해 전체적인 전기화학적 성능을 향상시킬 수 있다. 최근 연구에 의하면 3차원 기공성 이중채널 경로를 가지는 Zn전극은 이온 및 전하 전도가 균형을 이루어 수지상 형성을 억제하면서 가역적인 Zn2+ 전착/탈착을 가능하게 하였다[19]. 충방전 간 3차원 기공성 이중채널 Zn전극은 유효 면적당 전류밀도를 낮추어 Zn/Zn 대칭셀에서 3,500사이클 동안 낮은 과전압(60mV)을 보였다. V2O5/Zn 전지 테스트를 통해 일반적인 Zn호일형 전극보다 더 높은 비용량(443.4mAh/g), 수명 및 율속 특성을 나타내었다. Zn수지상 형성 문제뿐만 아니라 수계전해질 내에서의 Zn전극의 부식 문제도 해결해야 할 과제이다. 부식성이 있는 전해액에 대해 안정적인 음극 구조를 얻기 위해 부식에 약한 Zn에 부식 저항성이 큰 금속을 넣어 합금화시키는 방법들이 보고되고 있다. 이러한 합금화 전략은 부반응 부산물의 형성을 억제할 뿐만 아니라 균일한 Zn2+의 분포를 유도하고, 가역 용량을 증가시키고, Zn핵생성 에너지를 낮추면서 분극에 대한 과전압을 낮출 수 있다. 부식 저항성이 큰 구리를 넣어 만들어진 Cu/Zn 합금은 매우 높은 부식 저항성을 보여 이를 아연이온전지에 활용한 연구가 보고되었다[20]. 단순 Zn전극은 400mV의 높은 과전압을 나타낸 반면, Cu/Zn 합금 전극으로 제조된 대칭셀은 1mA/cm2의 전류밀도 및 0.5mAh/cm2 용량 조건하에서 거의 과전압 변화 없이 1,500사이클 동안 안정적으로 구동하였다. 음극 자체를 개질하는 방법 이외에도 음극/전해질 표면을 개질하여 가역적인 Zn금속 음극의 반응을 유도하는 연구들도 수행되어왔다. 이러한 연구들은 Zn금속 표면상에 인공적인 보호막을 형성시키는 것으로 한 예로 TiO2층을 Zn금속 표면상에 형성시켜 Zn의 부식을 억제하여 궁극적으로 부식 부산물 및 가스의 발생을 막고 쿨롱 효율을 높일 수 있었다[21]. 뿐만 아니라 인공적인 TiO2 보호층 도입을 통해 Zn/MnO2 셀이 3mAh/cm2의 전류밀도로 1,000사이클 후에도 85%의 용량 유지율을 보였다. 보호층의 다른 기능으로 기공성 구조를 도입하여 균일한 전해질 흐름을 제공하여 Zn전착률을 제어하는 방법이 보고되었다. Zn금속상에 코팅된 기공성 나노 CaCO3층은 Zn의 균일한 전착/탈착을 유도하였고 코팅층이 없는 Zn에 비해 1,000사이클 이후 42.7% 더 높은 방전용량(177 vs. 124mAh/g@1A/g)을 보였다[22].
Ⅴ. 결론
기존 리튬이온전지연구에서 얻어진 경험과 더불어 원료 소재의 풍부함, 저비용 공정, 높은 안전성, 및 환경 친화성 등의 장점으로 인하여 ESS용으로 적합한 아연이온전지에 대한 연구가 활발히 진행되고 있다. 그러나 아직은 대부분의 연구가 실험실 수준으로 실제 산업에 적용되기 위해서는 소재적인 면과 기술적인 면에서 많은 발전과 문제 해결이 요구된다. 본고에서는 아연이온전지의 주요 구성 요소인 전해질, 양극 및 음극 소재에 대한 기술적 동향을 살펴보았다. 물 기반의 수계전해질은 근본적으로 좁은 안정 전위창으로 인해 구동 전압이 낮아 에너지밀도의 저하가 불가피하기 때문에 안정성과 높은 이온전도성을 가지면서 물 분해반응을 억제할 수 있는 전해질 소재 개발 연구들이 수행되어왔다. 이를 위해서 고농도염 전략 등이 제안되어왔으나 소재 단가가 매우 높아 현실적인 해결책은 되지 못한다. 하이드로겔과 같은 고분자를 이용한 전해질 제조 방법은 물 분해반응을 억제하고 저비용 공정이기 때문에 대안으로 될 수 있으나 높은 이온전도도와 기계적 물성 확보가 필수적이다. 전해액 첨가제를 통해서도 구동 전압을 확장시킬 수 있고 전해질 안정성을 향상시킬 수 있기 때문에 전지시스템에 적합한 첨가제 소재의 개발이 요구된다. 양극으로 다양한 소재들이 개발되었고 그 특성을 향상시키는 연구들이 보고되었지만 에너지밀도를 높이기 위해서는 고전압에서 구동할 수 있는 양극 소재의 개발이 필수적이다. 음극 소재의 경우 전극 구조 제어와 보호막 코팅 등으로 성능이 향상되는 연구들이 많으나, 앞으로는 현실적인 적용을 위해 파우치 타입 전지에 적용이 가능한 대면적 공정 개발 및 적합한 소재 탐색이 필요하다. ESS용 아연이온전지 개발을 위해서는 소재부터 공정 개발까지 많은 시간과 노력이 필요하지만 기존 리튬이온전지에서 배운 경험을 바탕으로 그 개발 속도가 가속화될 것으로 전망된다.
용어해설
Solvation Sheath 용질 주위를 용매가 둘러싼 구조로, 예를 들면 수용액 내에서 양전하의 금속이온이 음전하의 산소 원자를 정전기적 인력으로 잡아당겨 물 분자가 껍질같이 금속이온을 둘러싸고 있는 현상
Hydrogel Electrolyte 물리적 또는 화학적인 결합을 통해 3차원적인 가교를 형성한 망상구조의 친수성 고분자가 금속염이 해리된 물을 함유한 상태로 금속이온을 전달하는 전해질로 활용됨
약어 정리
AMIBs
Aqueous Metal Ion Batteries
AZIBs
Aqueous Zinc Ion Batteries
DES
Deep Eutectic Solvent
DMSO
Dimethyl Sulfoxide
ESS
Energy Storage System
GHE
Gelatin Hydrogel Electrolyte
HPE
Hierarchical Polymer Electrolyte
PAA
Poly(acrylic acid)
PAM
Poly(acrylamide)
PEO
Poly(ethylene oxide)
PVA
Poly(vinyl alcohol)
X. Jia et al., "Active materials for aqueous zinc ion batteries: Synthesis, crystal structure, morphology, and electrochemistry," Chem. Rev., vol. 120, 2020, pp. 7795-7866.
V. Verma et al., "Progress in rechargeable aqueous zinc- and aluminum-ion battery electrodes: Challenges and outlook," Adv. Sustain. Syst., vol. 3, 2019, article no. 1800111.
N. Zhang et al., "Materials chemistry for rechargeable zinc-ion batteries," Chem. Soc. Rev., vol. 49, 2020, pp. 4203-4219.
Z. Liu et al., "Voltage issue of aqueous rechargeable metal-ion batteries," Chem. Soc. Rev., vol. 49, 2020, pp. 180-232.
V. Verma et al., "Undesired reactions in aqueous rechargeable zinc ion batteries," ACS Energy Lett., vol. 6, 2021, pp. 1773-1785.
N. Zhang et al., "Cation-deficient spinel ZnMn2O4 cathode in Zn(CF3SO3)2 electrolyte for rechargeable aqueous Zn-ion battery," J. Am. Chem. Soc., vol. 138, 2016, pp. 12894-12901.
L. Suo et al., ""Water-in-salt" electrolyte enables high-voltage aqueous lithium-ion chemistries," Science, vol. 350, 2015, pp. 938-943.
F. Wang et al., "Highly reversible zinc metal anode for aqueous batteries," Nat. Mater., vol. 17, 2018, pp. 543-549.
S. Karan et al., "Characterization of ion transport property in hot-press cast solid polymer electrolyte(SPE) films: [PEO: Zn(CF3SO3)2]," Ionics, vol. 23, 2017, pp. 2721-2726.
Q. Han et al., "Durable, flexible self-standing hydrogel electrolytes enabling high-safety rechargeable solidstate zinc metal batteries," J. Mater. Chem. A, vol. 6, 2018, pp. 23046-23054.
H. Li et al., "An extremely safe and wearable solidstate zinc ion battery based on a hierarchical structured polymer electrolyte," Energy Environ. Sci., vol. 11, 2018, pp. 941-951.
K. Wu et al., "Biodegradable gel electrolyte suppressing water-induced issues for long-life zinc metal anodes," ACS Appl. Mater. Interfaces, vol. 14, 2022, pp. 34612-34619.
F. Wan et al., "Aqueous rechargeable zinc/sodium vanadate batteries with enhanced performance from simultaneous insertion of dual carriers," Nat. Commun., vol. 9, 2018, article no. 1656.
L. Cao et al., "Solvation structure design for aqueous Zn metal batteries," J. Am. Chem. Soc., vol. 142, 2020, pp. 21404-21409.
H. Pan et al., "Reversible aqueous zinc/manganese oxide energy storage from conversion reactions," Nat. Energy, vol. 1, 2016, article no. 16039.
S. Khamsanga et al., "δ-MnO2 nanofower/graphite cathode for rechargeable aqueous zinc ion batteries," Sci. Rep., vol. 9, 2019, article no. 8441.
J. Zhou et al., "Investigation of V2O5 as a low-cost rechargeable aqueous zinc ion battery cathode," Chem. Commun., vol. 54, 2018, pp. 4457-4460.
X. Dai et al., "Freestanding graphene/VO2 composite films for highly stable aqueous Zn-ion batteries with superior rate performance," Energy Storage Mater., vol. 17, 2019, pp. 143-150.
W. Guo et al., "Dendrite-free Zn anode with dual channel 3D porous frameworks for rechargeable Zn batteries," Energy Storage Mater., vol. 30, 2020, pp. 104-112.
Z. Cai et al., "Chemically resistant Cu-Zn/Zn composite anode for long cycling aqueous batteries," Energy Storage Mater., vol. 27, 2020, pp. 205-211.
K. Zhao et al., "Ultrathin surface coating enables stabilized zinc metal anode," Adv. Mater. Interfaces, vol. 5, 2018, article no. 1800848.
그림 1
다양한 에너지 저장 장치 시스템의 중량당 출력 밀도 대 에너지 밀도 비교
출처 Reprinted with permission from [1], ⓒ 2022, American Chemical Society.

그림 2
(a) 기존 리튬이온전지와 수계형 아연이온전지 특성 비교, (b) 아연이온전지 구성 및 구동 메커니즘
출처 Reprinted with permission from [3], ⓒ 2020, Royal Society of Chemistry

그림 3
(a) Zn염에 따른 Zn/Zn 대칭셀 결과, (b) Zn염에 따른 Zn/Zn 대칭셀의 율속 및 장수명 결과
출처 Reproduced with permission from [6], ⓒ 2016, American Chemical Society.

그림 4
(a) Li+ 양이온 PSS 내 존재하는 물과 TFSI의 산소원자 수 및 Li+ 양이온에 주위의 자유로운 물의 비율, (b) 저농도와 고농도 염 전해질 내 Li+ 양이온의 PSS
출처 Reproduced with permission from [7].
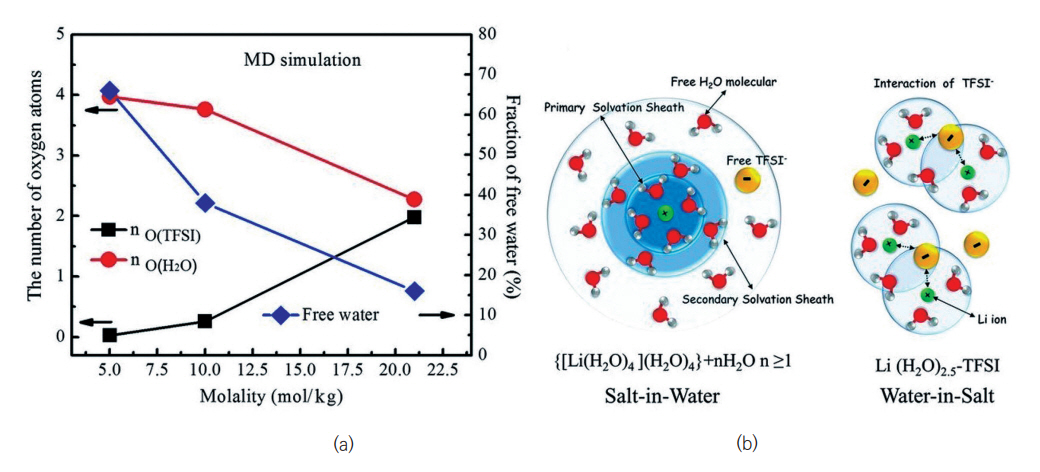
그림 5
아라비아검기반 겔 전해질의 수소환원 발생 억제 특성 및 아라비아검 전해질 이미지
출처 Reprinted with permission from [12], ⓒ 2022, American Chemical Society.

그림 6
(a) H2O와 H2O/DMSO에서의 Zn2+의 용매화 구조 비교, (b) DMSO 첨가제 효과에 대한 Zn/MnO2 셀의 수명 특성 결과 비교
출처 Reproduced with permission from [14], ⓒ 2014, American Chemical Society
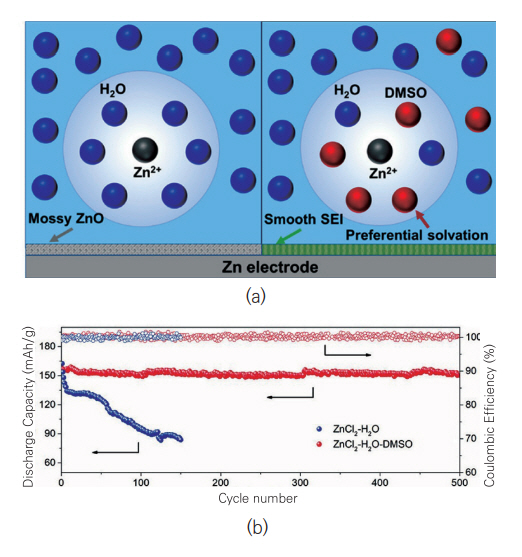
그림 7
대표적인 아연이온전지의 양극 소재의 구동전압대 비용량 그래프
출처 Reproduced with permission from [3], ⓒ 2020, Royal Society of Chemistry.
- Sign Up
- 전자통신동향분석 이메일 전자저널 구독을 원하시는 경우 정확한 이메일 주소를 입력하시기 바랍니다.