생분해 전자 소자 기술 개발 동향
Biodegradable Electronic Device Technology Development Trends
- 저자
-
김경현지능형부품센서연구실 khyun1@etri.re.kr 양용석지능형부품센서연구실 jullios@etri.re.kr 서동우소재부품연구본부 dwsuh@etri.re.kr
- 권호
- 39권 6호 (통권 211)
- 논문구분
- 차세대 소재부품 기술 동향
- 페이지
- 8-17
- 발행일자
- 2024.12.01
- DOI
- 10.22648/ETRI.2024.J.390602
 본 저작물은 공공누리 제4유형: 출처표시 + 상업적이용금지 + 변경금지 조건에 따라 이용할 수 있습니다.
본 저작물은 공공누리 제4유형: 출처표시 + 상업적이용금지 + 변경금지 조건에 따라 이용할 수 있습니다.- 초록
- With the rise of the digital age, the convenience of electronic devices has led to a rapid increase in electronic waste owing to growing demand. To address environmental pollution and foster a sustainable society, there is an increasing need for ecofriendly electronics that can decompose naturally. Biodegradable implantable electronic devices offer significant advantages in the medical field. These devices can degrade and be absorbed or excreted by the body, eliminating the need for surgical removal and thus reducing both surgical risks and the associated time and cost burdens. Recognizing this potential, extensive research and development efforts are currently underway. This report outlines the latest trends in biodegradable electronic devices, focusing on the degradation mechanisms and characteristics of the materials used, as well as their applications, structures, and the environments in which they operate. It also explores future directions and challenges in the development of biodegradable electronics.
Share
Ⅰ. 서론
현재 고도화된 전자산업의 발달로 인해서 인공지능반도체, HBM과 같은 최첨단의 전자 소자를 제작하고 적용하는 전자산업 주도의 사회가 되었다고 해도 과언이 아니다. 이러한 전자 소자는 기존의 전통적인 전자 산업 분야뿐만 아니라 의료, 자동차, 환경, 국방, 우주 등 산업 전체 분야로 확대되는 것을 확인할 수 있다. 그러나 이러한 전자 소자의 폭넓은 적용은 필연적으로 전자 산업 폐기물, 곧 전자 쓰레기를 증가시켜서 환경오염[1-3]과 저탄소 사회를 구현하는 데 상당한 걸림돌로 작용하고, 환경오염과 전자산업 폐기물을 처리하기 위한 비용 또한 지속해서 증가하고 있다. 이러한 문제를 해결하기 위해서는 친환경적이며 자연에서 자발적으로 분해되는 생분해 전자 소자에 관한 관심이 지속해서 증가하고 있다[4-6]. 생분해 전자 소자는 특히 의료 분야의 삽입형 의료 소자의 활용이 클 것으로 예상하는데, 왜냐하면 기존의 비생분해성 삽입형 전자 소자는 그 역할을 다한 후에 소자의 제거를 위해서 추가적인 수술이 필요하지만 생분해성 삽입형 전자 소자는 역할 후 스스로 분해되어 체내 흡수 및 배출되기 때문에 제거 수술이 필요 없고, 수술에 따른 위험 부담이 없으며, 시간적‧비용적 부담을 감소시킬 수 있는 장점이 있다[7-10]. 또한, 의료 분야 이외에도 높은 활용도가 예상되는 분야는 친환경 전자산업 분야와 정보 보안이 우선시 되는 국방 분야가 될 수 있다.
본고를 통해서 생분해 전자 소자의 다양한 응용 분야의 적용에 필요한 생분해 전자 소자를 구성하는 반도체, 전도체, 절연체 소재의 분해 특성과 전자 소자를 구성하는 구조 및 제작 방법에 대해서 언급하고 보다 구체적인 생분해 전자 소자의 응용 분야 및 향후 기술 전망에 대해서 다루고자 한다.
Ⅱ. 본론
1. 생분해 전자 소자 적용 소재의 분해 특성
생분해성 전자 소자를 구성하는 소재(반도체, 전도체, 절연체)들의 기본적인 분해 원리는 가수분해(Hydrolysis)다. 물 또는 식염수 용액이 소재의 표면에서 분해되면서 동시에 수용액이 물질 내부로 확산하는 가수분해가 지속해서 일어나는 반응성 확산(Reactive Diffusion)으로 일어난다[11].
가. 반도체 소재의 생분해
대표적인 반도체 소재인 실리콘(Si)은 기존의 벌크 웨이퍼 형태에서는 전기화학적으로 매우 느린 속도의 가수분해가 일어나는 것으로 알려져 있다. 실리콘의 가수분해 반응식은 다음과 같다[12].
생분해 전자 소자로 이용되는 초박막 형태의 나노멤브레인(NM: Nono Membrane) 구조나 나노 리본 구조를 이용하면, 단기간에 분해가 일어나도록 할 수 있다. 또한, pH, 온도, 이온 농도 등을 조절하여, 생분해 속도 제어가 가능하다고 보고되고 있다[13].
실리콘 나노멤브레인을 100nm 두께로 제작하여, 37℃ 식염수(pH 7.4)에 담가두었을 때, 약 24h 후에는 완전히 분해되는 것으로 보고되었다(그림 1). 또한, pH, 수용액의 이온 농도, 실리콘의 도핑 종류 및 도핑 농도에 따라서도 생분해 속도가 달라지는 것으로 확인되었다[14].
그림 1
100nm 실리콘 나노멤브레인의 37℃ 식염수에서의 시간에 따른 생분해성
출처 Reprinted with permission from S.W. Hwang et al., “Dissolution chemistry and biocompatibility of single-crystalline silicon nanomembranes and associated materials for transient electronics,” ACS Nano., vol. 8, 2014, pp. 5843-5851. Copyright 2014 American Chemical Society.

또한, 산화아연(ZnO)도 생분해 반도체 소재로 알려져 있으며, 생체적합성 소재로도 알려져 있다[15]. 생체에 적용 시 다양한 기계적 움직임을 이용하여 전기 에너지를 생산할 수 있어 전력 소자로서의 활용 가능성도 있는 것으로 알려져 있고, 가시광선 영역에서 투명하고, 높은 전자이동도를 가지고 있어, 다양한 광/전자 소자로서의 응용도 가능한 장점이 있다[16,17]. 실리콘 소재와 함께 생분해 전자 소자에 다양하게 활용이 가능할 것으로 예상한다. 산화아연(ZnO)의 가수분해 반응식은 다음과 같다[18].
나. 전도체(금속) 소재의 생분해
생분해 전도체 중 가장 많이 알려진 금속 소재는 마그네슘(Mg)일 것이다. 마그네슘(Mg)은 물과 반응성이 높아 가수분해 반응이 빠르게 일어나며, 반응식은 다음과 같다[19].
또한, 마그네슘(Mg)은 생분해 특성과 기계적 성질을 동시에 갖고 있으며, 생체적합성도 뛰어나 생분해성 도체 소재로 많이 활용되나 기존의 임플란트용 생체 재료로 사용되기에는 너무 쉽게 산화되어 분해되는 문제가 있다. 그래서 최근에는 합금 등으로 활용되어 사용 후 폐기물이나 생체 삽입 후 제거 수술 등이 필요치 않다는 장점이 있다. 생체액과 비슷한 수준의 상온의 식염수(Saline Solution, pH 7.4)에서 수일 내에 완전히 분해되는 것을 확인하였다.
또한, 마그네슘과 함께 생분해성 금속 소재로 관심을 가지는 소재는 텅스텐(W), 아연(Zn), 몰리브덴(Mo)이다. 각각의 생분해 반응식은 다음과 같다[20].
화학기상 증착(CVD)법으로 텅스텐(W) 박막을 형성하고, 포토 공정과 에칭 공정을 거쳐서 제작된 약 200nm 두께의 텅스텐(W) 박막 마이크로 패턴의 경우 상온의 탈이온화수(DI Water)에서 약 12일 후에 전도성 연결선으로의 기능을 상실했으며, 약 4주 후에 완전한 분해되는 것으로 보고되었다[21].
다. 폴리머 소재의 생분해
생분해 전자 소자의 기판으로 가장 많이 사용되는 폴리머 소재의 생분해에 대해서 크게 천연 고분자 재료와 합성 고분자 재료로 구분하여 설명하겠다. 고분자 재료는 고분자 매트릭스와 필러와 바인더로 구성되는데, 용매가 고분자에 침투하여 바인더 기능이 약화되면서 필러가 고분자 매트릭스에서 분리되면서 스웰링과 분해가 일어나게 된다[22,23]. 천연 고분자는 식물이나 동물에서 추출하는 것으로 가장 대표적인 것은 셀룰로오스(Cellulose), 녹말(Starch), 키토산(Chitosan), 젤라틴(Gelatin) 등이다. 이러한 천연 고분자 소재는 높은 생체 적합성과 생분해성을 가진다는 장점이 있어 많은 연구에서 생분해성 고분자를 제작하였고[24-27], 표 1은 생분해성 천연 고분자 재료들의 기계적 특성과 생분해 특성을 정리하였다[28-39].
표 1 천연 폴리머 소재의 기계적 및 생분해 특성
출처 김용우, 김경섭, 강승균, “시한성 전자소자를 위한 생분해성 기능성 무기/유기 하이브리드 복합재료,” 유연인쇄전자학술지, 제2권 제1호, 2023, pp. 25-45. [40].
그러나, 기계적 특성을 통해서 알 수 있듯이 천연 고분자 재료는 생체 적합성과 생분해성이 높은 장점은 있지만, 내구성과 유연성 및 신축성이 좋지 못한 단점이 있다. 이러한 천연 고분자 재료의 단점을 극복하고자 소재의 구조, 구성 및 고분자의 질량을 제어하여 합성 고분자 재료가 개발되었다. 합성 고분자 재료는 열에 대한 반응 특성에 따라 열가소성 고분자와 열경화성 고분자로 구분된다. 열가소성 고분자는 녹는점 이상으로 온도를 높이면 액체 상태로 녹고, 온도를 녹는점 이하로 낮추면 다시 고체 상태로 되돌아가는 소재를 말하고, 열경화성 고분자는 열이 가해졌을 때 녹지 않고 오히려 경화되는 특성을 가지는 고분자이다.
열가소성 고분자 소재로는 폴리 뷰틸렌 아디페이트 테레프탈레이트(PBAT: Poly(Butylene Adipate-co-Terephthalate)), 폴리 카프로 락톤(PCL: Poly CaproLactone), 폴리젖산(PLA: Poly Lactic Acid) 등이 있고, 열경화성 고분자 소재는 폴리언하이드라이드(PA: Poly Anhydride), 폴리글리세롤 세바케이트(PGS: Poly(Glycerol Sebacate)) 등이 있다[23,41-47]. 표 2는 생분해성 합성 고분자 소재들의 기계적 특성과 생분해 특성을 나타내었다[46,48-60].
표 2 합성 폴리머 소재의 기계적 및 생분해 특성
출처 김용우, 김경섭, 강승균, “시한성 전자소자를 위한 생분해성 기능성 무기/유기 하이브리드 복합재료,” 유연인쇄전자학술지, 제2권 제1호, 2023, pp. 25-45. [40].
2. 생분해성 전자 소자의 응용
생분해성 전자 장치의 궁극적인 목표는 인체에 이식하여 임상적인 측면에서 필요한 생체신호를 관찰하고 더 이상 필요하지 않으면 필요에 따라 분해할 수 있는 특성을 소재나 소자 레벨이 아니라 시스템 측면에서 시너지를 나타내는 것이다.
이에 따라 생체 내에서 단위 소자의 생체흡수성을 테스트한 연구는 상당히 많았지만, 장치나 시스템 레벨에서 속하는 여러 가지 다기능을 구현한 생체흡수성 소자(센서, 액추에이터, 전기 및 광학기기 등)를 포함하고 생체흡수성 형태로 상호 연결한 경우는 일부만 연구되었다.
이 부분에서는 두 개 이상의 서로 다른 생분해성 단위 소자를 상호 연결하여 다기능을 구현한 생분해성 전자 장치와 응용을 검토한다. 생체 내에서 테스트 된 생분해성 전자 장치와 특징 및 연구가 수행된 기관의 요약은 표 3에 나타내었다.
표 3 생분해성 전자 장치의 개발 동향
| 전자 장치 | 생분해 시스템 및 특징 | 연구 기관 |
|---|---|---|
| 생분해성 압력센싱 시스템 | 열적 성장한 SiO2 캡슐화 구조의 생분해 압력 센서 시스템(수명 > 25 days) | 미국 UIUC대 [61] |
| 생분해성 ICP 다중센싱 시스템 | 뇌의 외부 충격과 국소 출혈의 국소 압력, 온도 모니터링 시스템(수명 > 10 days) | 미국 UIUC대 [62] |
| 생분해성 화학센싱 시스템 | Au 나노막을 사용한 3 전극 구성의 전류 측정형과도 NO 센싱 시스템 | 중국 칭화대 [63] |
| 생분해성 마이크로 히팅 시스템 | 실크 기판 위에 Si NM 저항성 마이크로 히터 및 Mg 유도 코일 기반의 과도 열 요법 구현 시스템 | 미국 터프츠대 [64] |
| 생분해성 원격 트리거 시스템 | 호르몬 불균형, 악성 암, 골다공증 및 당뇨병 치료약물 전달용 일시적 원격 트리거 시스템 | 미국 노스 웨스턴대 [65] |
| 생분해성 다기능 스텐트 | 온도 측정/기록, 데이터 저장, 무선전송, 자극에 따라 약물을 방출할 수 있는 생체흡수성 스텐트 시스템 | 한국 IBS [66] |
| 무선 RF 전력 스캐빈저 시스템 | Mg RF 안테나, 인덕터, 커패시터, 저항기의 스캐빈저 회로(주파수: 950MHz, 전력: 54mW, 전력 변환 효율: 15.7%) | 미국 UIUC대 [67] |
| 생분해성 광전자 시스템 | 빛을 전달하는 광섬유, 빛 응답으로 전기 신호를 생성하는 광검출기, 광검출기를 외부 측정 설정에 전기적으로 상호 연결하기 위한 전극으로 구성된 시스템 | 미국 노스 웨스턴대 [68] |
생체에서 무기한으로 기능하고 온전한 상태를 유지하는 대부분의 기존 전자 장치와 달리 생분해성 전자 장치는 생체 내에서 완전히 분해되기 전에 정의된 안정적인 작동 기간을 특징으로 하는데, 이를 위해 가장 많이 연구된 것은 센서 및 모니터링 시스템이다.
이는 진단 또는 치료 기능의 제어된 조작 과정 중에 치유 및 감염과 같은 단기 생물학적 반응을 모니터링하기 위한 것이다. 그리고, 외부 장치의 장기 이식과 관련된 부작용이나 장치 제거를 위한 2차 수술 절차의 필요성을 피할 수 있는지도 고려된다. 이러한 생분해성 전자 장치를 성공적으로 사용하려면 모든 재료가 생체적합성이어야 하므로 이들의 가공성 및 분해 프로세스도 입증되어야 한다.
미국 UIUC대(일리노이 대학교 어배너-섐페인 캠퍼스)는 최근 임상 환경에서 사용되지 않지만, 장치 성능을 개선하기 위해 전 임상 환경에서 시험한 생분해성 전자 모니터링 시스템을 보고하였는데, 여기에서 열적으로 성장한 SiO2를 캡슐화 층으로 사용하여 쥐의 두개골 내 압력을 모니터링하는 압력 센서의 기능적 수명을 25일로 연장했다[61]. 이 시스템은 이전에 보고된 것보다 10배 이상 길었고, 임상 환경에서 사용하기에 더 적합하였다. 이와 함께 외상성 뇌 손상과 같은 잠복기가 있는 급성 질환을 모니터링하는 데 매우 유용한 생분해성 ICP 다중센싱 시스템이 연구되었다[62]. 뇌에 대한 외부 충격으로 인한 국소 출혈은 약 10일 동안 국소 압력을 계속 증가시킬 수 있는데, 초기 손상 후 나노 다공성 실리콘 및 PLGA 기반 생분해성 센서를 이용한 지속적인 두개골 내 압력 및 온도 모니터링은 외상성 뇌 손상 후 회복 진행 상황을 파악하는 데 매우 유용하였다.
중국 칭화대학교는 생분해성 화학 센서에 기반을 둔 과도 전자 장치를 개발하였는데 이는 또 다른 진단 분야로 적용할 수 있다[63]. 이 센서는 생분해성 기질들의 공중합체, 초박형 금 나노막 전극, 생체적 합성 필름으로 구성된 과도 NO 센서로 신경 전달 및 염증 반응의 모니터링에 적용되었다.
모니터링 이외에 생분해성 전자 장치는 생물학적 반응이나 신경 활동을 조절하거나 약물 전달을 유발하는 자극용으로도 개발되었다.
미국 터프츠대학교는 감염원을 제거하여 회복에 도움이 되는 열 요법의 용도로 실크 기판에 Si NM의 저항성 마이크로 히터가 있는 Mg의 유도 코일을 사용하는 초기 프로그래밍 가능한 생분해성 마이크로히팅 시스템을 개발하였다[64]. 이를 쥐의 피부 아래에 이식하여 24시간 후 박테리아 수의 현저한 감소 및 15일 후 완전한 용해의 성공적인 동작 결과를 보고하였다.
미국 노스웨스턴대학교는 약물 전달에 사용할 수 있는 생분해성 원격 트리거 시스템을 개발하였다[65]. 이는 호르몬 불균형, 악성 암, 골다공증 및 당뇨병 치료약물을 일시적으로 전달할 수 있도록 원격으로 트리거하는 기능을 가졌고, 2 × 2 배열의 상호 연결 구조에서 독립적인 트리거로 약물 누출을 보다 효과적으로 방지하였다.
한국 IBS 연구소는 흐름과 온도를 측정하고, 기록된 데이터를 저장 및 무선 전송하고, 자극에 따라 약물을 방출할 수 있는 생체흡수성 다기능 스텐트를 연구하였다[66]. 표준 생체흡수성 마그네슘-아연-망간 합금을 스텐트 메시 소재와 RF 안테나로, 생분해성을 갖는 저항성 온도 센서 및 열 저항성 흐름 센서로 구성됐고, 완성된 전자 소자의 추정 보유 시간은 수년이었다.
미국 UIUC대는 생분해성 전자 장치의 에너지원을 해결하기 위해 생분해성 무선 RF 전력 스캐빈저 시스템을 보고하였다[67]. 이 시스템은 반도체로 Si NM, 도체로 Mg의 RF 안테나, 인덕터, 커패시터, 저항기의 스캐빈저 회로로 구성되었고, 주파수 950MHz에서 전력 54mW, 전력 변환 효율 15.7%인 RF 안테나로 전력을 공급받았다. 모든 전자 재료는 실온에서 DI 내에서 생분해되며, 실크가 먼저 용해되고 나머지 재료는 시간이 지남에 따라 완전히 용해되면서 회로가 분해되었다.
미국 노스웨스턴대학교는 최근 생분해성 광전자 시스템을 보고하였는데, 이는 빛을 전달하는 데 사용되는 광섬유, 전달된 빛에 대한 응답으로 전기 신호를 생성하는 광검출기, 광검출기를 외부 측정 설정에 전기적으로 상호 연결하기 위한 전극으로 구성되었다[68]. 이 생분해성 분광기는 쥐의 뇌에 이식하여 10일 동안 안정적으로 작동한 후 성능이 저하되어 25일째에 시스템이 작동을 멈추었고, 살아 있는 동물에서 뇌 온도, 뇌 산소 포화도, 신경 활동을 지속적으로 감지할 가능성을 보여주었다.
3. 생분해성 전자 소자의 구조와 기능
앞서 언급된 생체 내에서 지정된 시간 동안 작동하는 생분해성 전자 장치를 제작하기 위해서는 표 4에 정리된 것처럼 반도체, 유전체 및 도체를 포함한 유무기 전자 재료의 생체적합성 등 다양한 요소와 기능을 고려해야 한다.
표 4 생분해성 전자 장치의 핵심재료와 구성요소 및 기능의 개발 동향
| 구성요소 | 생분해 구조 및 기능 | 연구 기관 |
|---|---|---|
| 생분해성 셀룰로오스 기판 | 생분해성 재료 기반의 초박형, 초경량 셀룰로오스 배리어층 및 기판 | 미국 스탠퍼드대 [69] |
| 생분해성 실리콘 구성요소 | 물에 완전한 용해 및 고성능, 확장 가능한 실리콘 기반 구성요소 | 미국 UIUC대 [70] |
| 생분해성 캡슐화 장벽구조 | 물 침투에 대한 우수한 소수성 유기 중합체와 무기 재료의 캡슐화/장벽층(PNIPAAM) | 아르헨티나 RCC대 [71] |
| 생분해성 전기자극 기능 | 기계적 신축성과 생체흡수성을 갖는 장수명, 신축성, 무선 생체흡수성 전기자극 기능 | 미국 노스 웨스턴대 [72] |
| 장기 동작 무선센싱 기능 | 동물 모델 내부의 표적 위치 추적용 Mg 인덕터 코일/커패시터 기반 생체흡수성 무선 센서 기능(수명 > 44 days) | 미국 노스 웨스턴대 [73] |
| 생분해성 약물 전달 기능 | LCR 회로로 구성된 원격 제어 약물 전달 기능 | 미국 터프츠대 [64] |
사용되는 재료의 용해 화학 및 동역학 성질은 온도, pH 및 이온 종과 같은 환경 요인에 따라 다양한 생체내 응용 분야에 적합한 회로 재료의 광범위한 조합으로 나타난다. 특히, 결정성, 다공성, 도핑 및 합금 구성과 같은 미세 구조적 요인은 재료 형성 과정을 통해 과도 소자의 용해 속도를 광범위하게 조정할 수 있다. 미국 스탠퍼드대학교는 생분해성 재료 기반의 초박형, 초경량 셀룰로오스 기판 및 배리어층으로 구성된 생분해성 셀룰로오스 기판을 제안하였다[69]. 미국 UIUC대는 실크 기질에 결정질 실리콘 나노막을 통합하여 물에 완전한 용해 및 고성능, 확장 가능한 실리콘 기반 구성요소를 개발하였다[70].
아르헨티나 RCC대는 물 침투에 대한 우수한 소수성 유기 중합체와 무기 재료의 캡슐화/장벽층(PNIPAAM)을 이용한 생분해성 캡슐화를 연구하였다[71]. 무기 및 유기 과도 캡슐화는 물 분자와 같은 증기의 확산을 제어하여 과도 소자의 기능적 수명을 원하는 시간 프레임까지 연장할 수 있다.
이와 같은 재료, 구성요소 및 캡슐화를 적용한 생분해성 전자 장치의 기능은 세 가지 측면에서 연구되었다.
미국 노스웨스턴대학교는 기계적 신축성과 생체흡수성을 갖는 장수명, 신축성 및 전기자극 기능을 보고하였다[72]. 이 생분해성 전기자극 기능은 생체에서 기계적 신축성과 최소한의 부기를 제공하는 생체흡수성 동적 공유 결합 폴리우레탄 소재를 사용하여 생체 내 실험에서 30일 동안 쥐 모델에서 좌골 신경의 장기간 지속할 수 있는 면에서 전기 자극 실험으로 입증되었다.
장기동작 무선센싱 기능은 동물 모델 내부의 표적 위치 추적용 Mg 인덕터 코일/커패시터 기반으로 제작되었고, 44일 이상의 장수명이 관찰되었다[73].
미국 터프츠대학교는 생분해성 LCR 회로로 구성된 회로로 원격 제어가 가능한 약물 전달 기능을 발표하였다[64]. 여기서 약물 방출 속도와 복용량은 생분해 소재의 결정성에 의존함을 밝혔다.
Ⅲ. 결론
생분해성 전자 장치는 지난 십여 년 동안 다양한 유형의 센서, 작동기 또는 다양한 기능을 가진 시스템의 형태로 구현되었다. 이것은 생체의학 응용 분야에서 일반적인 이식형 상용 장치와 비교하여 진단 및 치료에 실시간으로 거의 정확한 데이터/신호 분석을 가능하게 하는 특징 때문일 것이다.
게다가 생분해성 전자 장치는 이식된 전자 장치를 제거하기 위한 2차 수술을 하지 않을 수 있고, 일반적으로 생체흡수성 기판에 제작되며, 이는 초박형이고 자연스럽게 유연하여 장치와 생체 조직 간의 큰 기계적 불일치를 없애고 생체 조직의 수동적 손상 및 불편함을 줄인다.
그러나, 재료와 장치의 빠른 용해 속도를 조절하거나 원하는 동작 시간 동안 안정적인 에너지를 공급하는 것은 안정적인 작동 시간 측면에서 아직 해결해야 할 중요한 과제로 남아있다. 이것이 해결된 생분해성 전자 제품은 환경, 바이오, 의학 및 지속 가능한 전자공학 분야에서 차세대 시장의 훌륭한 발판이 될 것이다.
용어해설
생분해 전자 소자 전자 소자를 구성하는 모든 소재가 수분이나 토양에서 분해 가능하며 독성이나 오염이 거의 없는 전자 소자
생분해 반도체 나노멤브레인 기판이나 나노 리본 기판 등을 이용하여 생분해나 가수분해가 가능한 실리콘(Si), 산화아연(ZnO) 등의 반도체 소재
친환경 전자 소자 자연환경에 노출되었을 때, 생분해성, 무독성, 안정성 등의 문제가 매우 낮은 환경친화적인 전자 소자
약어 정리
ICP
IntraCranial Pressure
PA
Poly Anhydarid
PBAT
Poly(Butylene Adipate-co-Terephthalate)
PBS
Phosphate-Buffered Saline
PCL
Poly CaproLactone
PEO
Poly(Ethylene Oxide)
PGS
Poly(Glycerol Sebacate)
PLA
Poly Lactic Acid
PLGA
Poly(Lactic-co-Glycolic Acid)
PNIPAAM
Poly(N-isopropylacrylamide)
PVA
Ploy(Vinyl Alcohol)
H. Hosono et al., "Room-temperature fabrication of transparent flexible thin-film transistors using amorphous oxide semiconductors," Nature, vol. 432, 2004, pp. 488-492.
A. Javey et al., "Fully integrated wearable sensor arrays for multiplexed in situ perspiration analysis," Nature, vol. 529, 2016, pp. 509-514.
S.K. Kang, L. Yin, and C. Bettinger, "The emergence of transient electronic devices," MRS Bull. vol. 45, no. 2, 2020, pp. 87-95.
Z. Ma et al., "High-performance green flexible electronics based on biodegradable cellulose nanofibril paper," Nat. Commun., vol. 6, 2015. doi: 10.1038/ncomms8170
Z. Bao et al., "Biodegradable polymeric materials in degradable electronic devices," ACS Cent. Sci., vol. 4, no. 3, 2018, pp. 337-348.
M.V. Chinnamani et al., "A composite microfiber for biodegradable stretchable electronics," Micromach., vol. 12, 2021. doi: 10.3390/mi12091036
J.S. Lee et al., "Biodegradable metallic glass for stretchable transient electronics," Adv. Sci., vol. 8, no. 10, 2021. doi: 10.1002/advs.202004029
K.B. Lee et al., "Fully implantable and bioresorbable cardiac pacemakers without leads or batteries," Nat. Biotechnol. vol. 39, 2021, pp. 1228-1238.
D.H. Kim et al., "Flexible and biodegradable electronic implants for diagnosis and treatment of brain diseases." Curr. Opin. Biotechnol. vol. 72, 2021, pp. 13-21.
C. Fernandes and I. Taurino, "Biodegradable molybdenum (Mo) and tungsten (W) devices: One step closer towards fully-transient biomedical implants," Sensors, vol. 22, no. 8, 2022. doi: 10.3390/s22083062
J.A. Rogers et al., "An analytical model of reactive diffusion for transient electronics," Adv. Funct. Mater., vol. 23, 2013. pp. 3106-3114.
H. Luan et al., "Skin-integrated wireless haptic interfaces for virtual and augmented reality," Nature, vol. 575, 2019, pp. 473-479.
S.W. Hwang et al., "25th anniversary article: Materials for high-performance biodegradable semiconductor devices," Adv. Mater., vol. 26, 2014, pp. 1992-2000.
S.W. Hwang et al., "Dissolution chemistry and biocompatibility of single-crystalline silicon nanomembranes and associated materials for transient electronics," ACS nano., vol. 8, 2014, pp. 5843-5851.
D.L. Kaplan et al., "Macrophage responses to silk," Biomaterials, vol. 24, 2003, pp. 3079-3085.
P. Mitra et al., "Preparation of Al-doped ZnO (AZO) thin film by SILAR," J. Phys. Sci., vol. 12, 2008, pp. 221-229.
K. Miyamoto et al., "High-electron-mobility ZnO epilayers grown by plasma assisted molecular beam epitaxy," J. Cryst. Growth., vol. 265, 2004, pp. 34-40.
M.H. Wong et al., "Electronic waste management approaches: an overview," Waste Manage., vol. 33, 2013, pp. 1237-1250.
X. Xie et al., "Dissolvable metals for transient electronics," Adv. Funct. Mater., vol. 24, 2014, pp. 645-658.
J.A. Rogers et al., "Materials and fabrication sequences for water soluble silicon integrated circuits at the 90 nm node," Appl. Phys. Lett., vol. 106, 2015. doi: 10.1063/1.4905321
S.W. Hwang et al., "Materials and fabrication strategies for biocompatible and biodegradable conductive polymer composites toward bio-integrated electronic systems," Adv. Sustainable Syst., vol. 6, no. 2, 2022. doi: 10.1002/adsu.202100075
J.Y. Lee et al., "Biodegradable molybdenum/polybutylene adipate terephthalate conductive paste for flexible and stretchable transient electronics," Adv. Mater. Technol., vol. 7, no. 2, 2022. doi: 10.1002/admt.202001297
G.B. Kim et al., "Isotropic conductive paste for bioresorbable electronics," Materials Today Bio., vol. 18, 2023. doi: 10.1016/j.mtbio.2023.100541
S. Min et al., "Natural wax for transient electronics," Adv. Funct. Mater., vol. 28, no. 32, 2018. doi: 10.1002/adfm.201801819
C. Xiong et al., "Chitin/MoS2 nanosheet dielectric composite films with significantly enhanced discharge energy density and efficiency," Biomacromolecules, vol. 21, 2020, pp. 2929-2937.
J. Cheng et al., "Materials, designs, and operational characteristics for fully biodegradable primary batteries," Adv. Mater., vol. 26, no. 23, 2014, pp. 3879-3884.
V. Dmitriev et al., "Nanomechanical and structural properties of native cellulose under compressive stress," Biomacromolecules, vol. 12, no. 6, 2011, pp. 2178-2183.
J. Zhang et al.,"Graphene oxide/cellulose composite films with enhanced UV-shielding and mechanical properties prepared in NaOH/Urea aqueous solution," RSC Adv., vol. 6, 2016, pp. 73358-73364.
R. Laskowski et al., "Cellulose decomposed faster in fallow soil than in meadow soil due to a shorter lag time," J. Soils Sediments, vol. 17, 2017, pp. 299-305.
R.A. Ilyas et al., "Development and characterization of cornstarch-based bioplastics packaging film using a combination of different plasticizers," Polymers, vol. 13, no. 20, 2021. doi: 10.3390/polym13203487
C.J. Ulhoa et al., "Immobilization of cryptococcus flavus α-amylase on glass tubes and its application in starch hydrolysis," Starch-Stärke, vol. 69, no. 3-4, 2017. doi: 10.1002/star.201600189
C. Pechyen et al., "Physico-chemical properties of ZnO and chitosan composite for packaging material," J. Biobased Mater. Bioenergy, vol. 11, no. 3, 2017, pp. 183-192.
M.O. Taha et al., "Degradability of chitosan micro/nanoparticles for pulmonary drug delivery," Heliyon, vol. 5, 2019. doi: 10.1016/j.heliyon.2019.e01684
Z. He et al., "Effects of cellulose nanofibers filling and palmitic acid emulsions coating on the physical properties of fish gelatin films," Food Biophys., vol. 12, 2017, pp. 23-32.
P. Surin et al., "In vitro degradation of gelatin/carboxymethylcellulose scaffolds for skin tissue regeneration," Chem. Eng. Trans., vol. 74, 2019, pp. 1555-1560.
C. Ketata et al., "Experimental study of physical and mechanical properties of natural and synthetic waxes using uniaxial compressive strength test," in Proc. Third Int. Conf. Modeling, Simulations Appl. Optim., Sharhag, UAE, 2019, pp. 1-5.
F. Anguebes-Franceschi et al., "Characterization of beeswax, candelilla wax, and paraffin wax for coating cheeses," Coatings, vol. 11, no. 3, 2021. doi: 10.3390/coatings11030261
A.O. Hanstveit et al., "Biodegradability of petroleum waxes and beeswax in an adapted CO2 evolution test," Chemosphere, vol. 25, no. 4, 1992, pp. 605-620.
Y.Y. Chen et al., "Metal microparticle-polymer composites as printable, bio/ecoresorbable conductive inks," Materials Today, vol. 21, no.3, 2018, pp. 207-215.
J.A. Rogers et al., "Room temperature elec trochemical sintering of Zn microparticles and its use in printable conducting Inks for bioresorbable electronics," Adv. Mater., vol. 29, no. 38, 2017. doi: 10.1002/adma.201702665
S. Choudhary, "Characterization of amorphous silica nanofiller effect on the structural, morphological, optical, thermal, dielectric and electrical properties of PVA-PVP blend based polymer nanocomposites for their flexible nanodielectric applications," J. Mater. Sci. Mater. Electron., vol. 29, 2018, pp. 10517-10534.
G.L. Whiting et al., "Poly(Lactic Acid)-based ink for biodegradable printed electronics with conductivity enhanced through solvent aging," ACS Appl. Mater. Interfaces, vol. 12, no. 23, 2020, pp. 23494-23501.
I. Noshadi et al., "Synthesized biocompatible and conductive ink for 3D printing of flexible electronics," J. Mech. Behav. Biomed. Mater., vol. 110, 2020. doi: 10.1016/j.jmbbm.2020.103960
J.F. Cortes et al., "Biodegradable materials for multilayer transient printed circuit boards," Adv. Mater., vol. 26, no. 43, 2014, pp. 7371-7377.
M. Bassyouni et al., "Recent advances in biodegradable polymers for sustainable applications," npj Mater. Degrad., vol. 6, 2022. doi: 10.1038/s41529-022-00277-7
J. Chaishome et al., "Tensile properties of PLA/PBAT blends and PLA fibre-reinforced PBAT composite," MATEC Web Conf., 2018. doi: 10.1051/matecconf/201819203014
A. Kanwal et al., "Degradation of poly(butylene adipate-co-terephthalate) by Stenotrophomonas sp. YCJ1 isolated from farmland soil," J. Environ. Sci., vol. 103, 2021, pp. 50-58.
C. Tonda-Turo et al., "Biocompatible electrospun polycaprolactone-polyaniline scaffold treated with atmospheric plasma to improve hydrophilicity," Bioengineering, vol. 8, no. 2, 2021. doi: 10.3390/bioengineering8020024
A.C. Albertsson "Crucial Differences in the hydrolytic degradation between industrial polylactide and laboratory-scale poly(L-lactide)," ACS Appl. Mater. Interfaces, vol. 4, no. 5, 2012, pp. 2788-2793.
L. Li et al., "A cross-linked poly(ethylene oxide)-based electrolyte for all-solid-state lithium metal batteries with long cycling stability," Front. Mater., 2022. doi: 10.3389/fmats.2022.864478
J. Saremi et al., "Fabrication of chitosan-polyvinyl alcohol and silk electrospun fiber seeded with differentiated keratinocyte for skin tissue regeneration in animal wound model," J. Biol. Eng., vol. 14, 2020. doi: 10.1186/s13036-020-00249-y
H.T. Sasmazel et al., "Core/shell glycine-polyvinyl alcohol/polycaprolactone nanofibrous membrane intended for guided bone regeneration: Development and characterization," Coatings, vol. 11, no. 9, 2021. doi: 10.3390/coatings11091130
W. Park et al., "Effect of various shaped magnesium hydroxide particles on mechanical and biological properties of poly(lactic-co-glycolic acid) composites," J. Ind. Eng. Chem., vol. 59, 2018, pp. 266-276.
A. Saiani et al., "Degradation kinetics of poly(lactic-co-glycolic) acid block copolymer cast films in phosphate buffer solution as revealed by infrared and Raman spectroscopies," Polym. Degrad. Stab., vol. 96, no. 10, 2011, pp. 1882-1889.
L.E. Janes et al., "Advanced materials in wireless, implantable electrical stimulators that offer rapid rates of bioresorption for peripheral axon regeneration," Adv. Funct. Mater., vol. 31, no. 29, 2021. doi: 10.1002/adfm.202102724
D.F. Newgreen et al., "Nonlinear easticity of core/shell spun PGS/PLLA fibres and their effect on cell proliferation," Biomaterials, vol. 34, no. 27, 2013, pp. 6306-6317.
W. Zhang et al., "Biomimetic poly(glycerol sebacate)/polycaprolactone blend scaffolds for cartilage tissue engineering," J. Mater. Sci. Mater. Med., vol. 30, 2019. doi: 10.1007/s10856-019-6257-3
S. Ebrahimi-Barough, "In vivo investigation of PCL/PHBV/hydroxyapatite nanocomposite scaffold in regeneration of critical-sized bone defects," Fibers Polym., vol. 22, 2021, pp. 2507-2516.
J. Shin et al., "Bioresorbable pressure sensors protected with thermally grown silicon dioxide for the monitoring of chronic diseases and healing processes," Nat. Biomed. Eng., vol. 3, 2019, pp. 37-46.
S. K. Kang et al., "Bioresorbable silicon electronic sensors for the brain," Nature, vol. 530, 2016, pp. 71-76.
R. Li et al., "A flexible and physically transient electrochemical sensor for real-time wireless nitric oxide monitoring," Nat. Commun., vol. 11, 2020. doi: 10.1038/s41467-020-17008-8
H. Tao et al., "Silk-based resorbable electronic devices for remotely controlled therapy and in vivo infection abatement," Proc. Natl. Acad. Sci. USA, vol. 111, 2014, pp. 17385-17389.
J. Koo et al., "Wirelessly controlled, bioresorbable drug delivery device with active valves that exploit electrochemically triggered crevice corrosion," Sci. Adv., vol. 6, 2020. doi: 10.1126/sciadv.abb1093
D. Son et al., "Bioresorbable Electronic Stent Integrated with Therapeutic Nanoparticles for Endovascular Diseases," ACS Nano, vol. 9, no. 6, 2015, pp. 5937-5946.
S.W. Hwang et al., "Materials for bioresorbable radio frequency electronics," Adv. Mater., vol. 25, 2013, pp. 3526-3531.
W. Bai et al., "Bioresorbable photonic devices for the spectroscopic characterization of physiological status and neural activity," Nat. Biomed. Eng., vol. 3, no. 6, 2019, pp. 644-654.
T. Lei et al., "Biocompatible and totally disintegrable semiconducting polymer for ultrathin and ultralightweight transient electronics," Proc. Natl. Acad. Sci. USA, vol. 114, 2017. doi: 10.1073/pnas.1701478114
S.-W. Hwang et al., "A Physically Transient Form of Silicon Electronics," Sci., vol. 337, 2012, pp. 1640-1644.
V. Capella et al., "Cytotoxicity and bioadhesive properties of poly-N-isopropylacrylamide hydrogel," Heliyon, vol. 5, no. 4, 2019. doi: 10.1016/j.heliyon.2019.e01474
Y.S. Choi et al., "Stretchable, dynamic covalent polymers for soft, long-lived bioresorbable electronic stimulators designed to facilitate neuromuscular regeneration," Nat. Commun., vol. 11, 2020. doi: 10.1038/s41467-020-19660-6
D. Lu et al., "Bioresorbable wireless sensors as temporary implants for in vivo measurements of pressure," Adv. Funct. Mater., vol. 30, 2020. doi: 10.1002/adfm.202003754
그림 1
100nm 실리콘 나노멤브레인의 37℃ 식염수에서의 시간에 따른 생분해성
출처 Reprinted with permission from S.W. Hwang et al., “Dissolution chemistry and biocompatibility of single-crystalline silicon nanomembranes and associated materials for transient electronics,” ACS Nano., vol. 8, 2014, pp. 5843-5851. Copyright 2014 American Chemical Society.
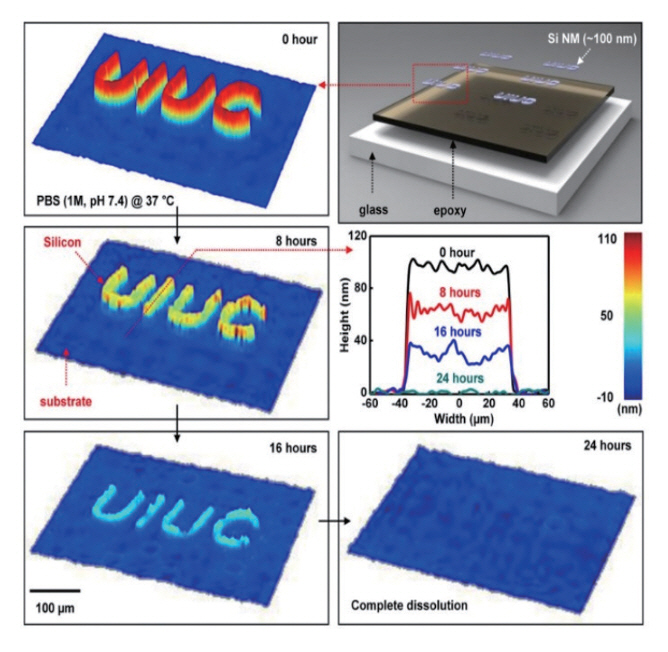
표 1 천연 폴리머 소재의 기계적 및 생분해 특성
출처 김용우, 김경섭, 강승균, “시한성 전자소자를 위한 생분해성 기능성 무기/유기 하이브리드 복합재료,” 유연인쇄전자학술지, 제2권 제1호, 2023, pp. 25-45. [40].
표 2 합성 폴리머 소재의 기계적 및 생분해 특성
출처 김용우, 김경섭, 강승균, “시한성 전자소자를 위한 생분해성 기능성 무기/유기 하이브리드 복합재료,” 유연인쇄전자학술지, 제2권 제1호, 2023, pp. 25-45. [40].
표 3 생분해성 전자 장치의 개발 동향
| 전자 장치 | 생분해 시스템 및 특징 | 연구 기관 |
|---|---|---|
| 생분해성 압력센싱 시스템 | 열적 성장한 SiO2 캡슐화 구조의 생분해 압력 센서 시스템(수명 > 25 days) | 미국 UIUC대 [61] |
| 생분해성 ICP 다중센싱 시스템 | 뇌의 외부 충격과 국소 출혈의 국소 압력, 온도 모니터링 시스템(수명 > 10 days) | 미국 UIUC대 [62] |
| 생분해성 화학센싱 시스템 | Au 나노막을 사용한 3 전극 구성의 전류 측정형과도 NO 센싱 시스템 | 중국 칭화대 [63] |
| 생분해성 마이크로 히팅 시스템 | 실크 기판 위에 Si NM 저항성 마이크로 히터 및 Mg 유도 코일 기반의 과도 열 요법 구현 시스템 | 미국 터프츠대 [64] |
| 생분해성 원격 트리거 시스템 | 호르몬 불균형, 악성 암, 골다공증 및 당뇨병 치료약물 전달용 일시적 원격 트리거 시스템 | 미국 노스 웨스턴대 [65] |
| 생분해성 다기능 스텐트 | 온도 측정/기록, 데이터 저장, 무선전송, 자극에 따라 약물을 방출할 수 있는 생체흡수성 스텐트 시스템 | 한국 IBS [66] |
| 무선 RF 전력 스캐빈저 시스템 | Mg RF 안테나, 인덕터, 커패시터, 저항기의 스캐빈저 회로(주파수: 950MHz, 전력: 54mW, 전력 변환 효율: 15.7%) | 미국 UIUC대 [67] |
| 생분해성 광전자 시스템 | 빛을 전달하는 광섬유, 빛 응답으로 전기 신호를 생성하는 광검출기, 광검출기를 외부 측정 설정에 전기적으로 상호 연결하기 위한 전극으로 구성된 시스템 | 미국 노스 웨스턴대 [68] |
표 4 생분해성 전자 장치의 핵심재료와 구성요소 및 기능의 개발 동향
| 구성요소 | 생분해 구조 및 기능 | 연구 기관 |
|---|---|---|
| 생분해성 셀룰로오스 기판 | 생분해성 재료 기반의 초박형, 초경량 셀룰로오스 배리어층 및 기판 | 미국 스탠퍼드대 [69] |
| 생분해성 실리콘 구성요소 | 물에 완전한 용해 및 고성능, 확장 가능한 실리콘 기반 구성요소 | 미국 UIUC대 [70] |
| 생분해성 캡슐화 장벽구조 | 물 침투에 대한 우수한 소수성 유기 중합체와 무기 재료의 캡슐화/장벽층(PNIPAAM) | 아르헨티나 RCC대 [71] |
| 생분해성 전기자극 기능 | 기계적 신축성과 생체흡수성을 갖는 장수명, 신축성, 무선 생체흡수성 전기자극 기능 | 미국 노스 웨스턴대 [72] |
| 장기 동작 무선센싱 기능 | 동물 모델 내부의 표적 위치 추적용 Mg 인덕터 코일/커패시터 기반 생체흡수성 무선 센서 기능(수명 > 44 days) | 미국 노스 웨스턴대 [73] |
| 생분해성 약물 전달 기능 | LCR 회로로 구성된 원격 제어 약물 전달 기능 | 미국 터프츠대 [64] |
- Sign Up
- 전자통신동향분석 이메일 전자저널 구독을 원하시는 경우 정확한 이메일 주소를 입력하시기 바랍니다.